Ajánlások COPD-s betegek számára. Hoble - nemzeti ajánlások
A COPD (krónikus obstruktív tüdőbetegség) osztályozása széles, és tartalmazza a betegség leggyakoribb stádiumainak és változatainak leírását, amelyekben előfordul. És bár nem minden betegnél halad a COPD ugyanazon forgatókönyv szerint, és nem mindenki azonosítható egy bizonyos típusként, a besorolás mindig releváns marad: a legtöbb beteg belefér.
A COPD szakaszai
Az első osztályozást (COPD spirográfiai osztályozás), amely meghatározta a COPD stádiumait és kritériumait, még 1997-ben javasolta a tudósok egy csoportja, amely a World COPD Initiative nevű bizottságban egyesült (angolul a név így hangzik: „Global Initiative for krónikus). Obstruktív tüdőbetegség" és rövidítve GOLD). Elmondása szerint négy fő szakasz van, amelyek mindegyikét elsősorban a FEV - vagyis a kényszerített kilégzési áramlás térfogata az első másodpercben - határozza meg:
- A COPD 1 foka nem különbözik a speciális tünetekben. A hörgők lumenje eléggé beszűkült, a légáramlás sem túl észrevehetően korlátozott. A beteg nem tapasztal nehézségeket a mindennapi életben, légszomjat csak aktív fizikai megterheléskor, nedves köhögést - csak alkalmanként, nagy valószínűséggel éjszaka tapasztal. Ebben a szakaszban kevesen fordulnak orvoshoz, általában más betegségek miatt.
- A COPD 2 foka kifejezettebbé válik. A légszomj azonnal kezdődik, amikor fizikai tevékenységet próbálnak végezni, reggel köhögés jelenik meg, amelyet észrevehető köpet - néha gennyes - kísér. A beteg észreveszi, hogy kevésbé szívós, és ismétlődő légúti betegségekben kezd szenvedni - az egyszerű SARS-től a hörghurutig és a tüdőgyulladásig. Ha az orvoshoz fordulás oka nem a COPD gyanúja, akkor előbb-utóbb mégis az egyidejű fertőzések miatt kerül hozzá a beteg.
- A COPD 3. fokozatát nehéz szakasznak nevezik - ha a betegnek elég ereje van, kérheti a rokkantság megállapítását, és magabiztosan várja, hogy kiállítsák a számára igazolást. A légszomj kisebb fizikai megterhelés esetén is jelentkezik – egészen a lépcsőn való felmászáshoz. A beteg szédül, sötét a szeme. A köhögés gyakrabban, legalább havonta kétszer jelentkezik, paroxizmális jellegűvé válik, és mellkasi fájdalmak kísérik. Ugyanakkor a megjelenés megváltozik - a mellkas kitágul, a vénák megduzzadnak a nyakon, a bőr színe cianotikusra vagy rózsaszínesre változik. A testtömeg vagy hirtelen csökken, vagy élesen csökken.
- A COPD 4. stádiuma azt jelenti, hogy minden munkaképességről megfeledkezhet - a beteg tüdejébe belépő légáramlás nem haladja meg a szükséges térfogat harminc százalékát. Bármilyen fizikai erőfeszítés – az átöltözésig vagy a higiéniai eljárásokig – légszomjat, zihálást a mellkasban, szédülést okoz. Maga a légzés nehéz, fáradságos. A páciensnek folyamatosan oxigénpalackot kell használnia. A legrosszabb esetekben kórházi kezelésre van szükség.
A GOLD azonban 2011-ben arra a következtetésre jutott, hogy az ilyen kritériumok túlságosan homályosak, és helytelen pusztán a spirometria (amely meghatározza a kilégzés mennyiségét) alapján diagnózist felállítani. Ráadásul nem minden betegnél alakult ki a betegség egymás után, enyhe stádiumtól súlyos stádiumig – sok esetben lehetetlen volt meghatározni a COPD stádiumát. CAT kérdőívet dolgoztak ki, amelyet maga a beteg tölt ki, és lehetővé teszi az állapot pontosabb meghatározását. Ebben a betegnek egytől ötig terjedő skálán kell meghatároznia, hogy mennyire kifejezettek a tünetei:
- köhögés - egy megfelel a "nincs köhögés" kijelentésnek, öt "állandóan";
- köpet - egy „nincs köpet”, öt „folyamatosan jön ki a köpet”;
- szorító érzés a mellkasban - „nem” és „nagyon erős”;
- légszomj - az "egyáltalán nincs légszomj"-tól a "legcsekélyebb megerőltetéssel jelentkező légszomjig";
- háztartási tevékenység - "korlátozások nélkül" a "nagyon korlátozott"-ig;
- elhagyni a házat - a "szükségből magabiztosan" a "nem is szükségből";
- alvás - a "jó alvástól" az "álmatlanságig";
- energia - "tele van energiával" az "egyáltalán nincs energia".
Az eredményt pontozással határozzák meg. Ha tíznél kevesebb van belőlük, a betegség szinte semmilyen hatással nincs a beteg életére. Húsznál kevesebb, de tíznél több - mérsékelt hatású. Harmincnál kevesebb – erős befolyással bír. Több mint harminc – óriási hatással van az életre.
Figyelembe veszik a páciens állapotának objektív mutatóit is, amelyek műszerekkel rögzíthetők. A főbbek az oxigénfeszültség és a hemoglobin telítettség. Egészséges embernél az első érték nem esik nyolcvan alá, a második pedig nem esik kilencven alá. A betegeknél az állapot súlyosságától függően a számok eltérőek:
- viszonylag enyhe - akár nyolcvan-kilencvenig a tünetek jelenlétében;
- közepes súlyosság esetén - hatvan-nyolcvanig;
- súlyos esetekben - kevesebb, mint negyven és körülbelül hetvenöt.
 2011 után a GOLD szerint a COPD-nek már nincsenek szakaszai. Csak súlyossági fokok vannak, amelyek azt jelzik, hogy mennyi levegő jut be a tüdőbe. És a beteg állapotára vonatkozó általános következtetés nem úgy néz ki, hogy „a COPD egy bizonyos stádiumában van”, hanem „egy bizonyos kockázati csoportba tartozik a COPD súlyosbodása, káros hatásai és halálozása szempontjából”. Összesen négyen vannak.
2011 után a GOLD szerint a COPD-nek már nincsenek szakaszai. Csak súlyossági fokok vannak, amelyek azt jelzik, hogy mennyi levegő jut be a tüdőbe. És a beteg állapotára vonatkozó általános következtetés nem úgy néz ki, hogy „a COPD egy bizonyos stádiumában van”, hanem „egy bizonyos kockázati csoportba tartozik a COPD súlyosbodása, káros hatásai és halálozása szempontjából”. Összesen négyen vannak.
- A csoport – alacsony kockázat, kevés tünet. Ebbe a csoportba tartozik az a beteg, akinek egy éven belül legfeljebb egy exacerbációja volt, a CAT-en tíznél kevesebb pontot ért el, légszomj pedig csak terheléskor jelentkezik.
- B csoport - alacsony kockázat, sok tünet. A beteg akkor tartozik abba a csoportba, ha nem volt egynél több exacerbáció, de gyakran jelentkezik légszomj, és a CAT-en tíznél több pontot értek el.
- C csoport - magas kockázat, kevés tünet. Abba a csoportba tartozik az a beteg, aki évente egynél több exacerbációja volt, terhelés közben nehézlégzés lép fel, és a CAT pontszáma tíz pont alatt van.
- D csoport - magas kockázat, sok tünet. Egynél több exacerbáció, légszomj lép fel a legkisebb megerőltetésre, és több mint tíz pont a CAT-nél.
Az osztályozás, bár úgy készült, hogy a lehető legnagyobb mértékben figyelembe vegye az adott beteg állapotát, mégsem tartalmazott két olyan fontos mutatót, amely befolyásolja a beteg életét, és a diagnózisban szerepel. Ezek a COPD fenotípusai és társbetegségei.
A COPD fenotípusai
 A krónikus obstruktív tüdőbetegségben két fő fenotípus határozza meg a beteg megjelenését és a betegség előrehaladását.
A krónikus obstruktív tüdőbetegségben két fő fenotípus határozza meg a beteg megjelenését és a betegség előrehaladását.
bronchitis típusa:
- Ok. Ennek oka a krónikus hörghurut, amelynek visszaesése legalább két évig előfordul.
- Változások a tüdőben. A fluorográfia azt mutatja, hogy a hörgők fala megvastagodott. A spirometrián látható, hogy a légáramlás gyengül, és csak részben jut be a tüdőbe.
- A felfedezés klasszikus kora ötven vagy annál idősebb.
- A páciens megjelenésének jellemzői. A beteg bőrszíne kifejezett cianotikus, mellkasa hordó alakú, testsúlya általában nő a fokozott étvágy miatt, és megközelítheti az elhízás határát.
- A fő tünet a köhögés, paroxizmális, bőséges gennyes köpet.
- Fertőzések - gyakran, mert a hörgők nem képesek kiszűrni a kórokozót.
- A szívizom "cor pulmonale" típusú deformációja - gyakran.
A Cor pulmonale egy olyan kísérő tünet, amelyben a jobb kamra megnagyobbodása és a szívverés felgyorsul – így a szervezet igyekszik kompenzálni a vér oxigénhiányát:
- röntgen. Látható, hogy a szív deformálódik és megnagyobbodik, és a tüdő mintázata fokozódik.
- A tüdő diffúz kapacitása - vagyis az az idő, amely alatt a gázmolekulák belépnek a vérbe. Általában, ha csökken, akkor nem sokat.
- Előrejelzés. A statisztikák szerint a bronchitis típusának magasabb a halálozási aránya.
Az emberek a hörghurut típusát „kék ödémának” nevezik, és ez meglehetősen pontos leírás - az ilyen típusú COPD-s beteg általában halványkék, túlsúlyos, állandóan köhög, de éber - a légszomj nem érinti őt annyira, mint a betegeket másik típus.
 tüdőtágulásos típus:
tüdőtágulásos típus:
- Ok. Az ok a krónikus emfizéma.
- Változások a tüdőben. A fluorográfián jól látható, hogy az alveolusok közötti válaszfalak megsemmisülnek, és levegővel töltött üregek keletkeznek - bullák. A spirometriával hiperventillációt rögzítenek - az oxigén bejut a tüdőbe, de nem szívódik fel a vérbe.
- A felfedezés klasszikus kora hatvan vagy annál idősebb.
- A páciens megjelenésének jellemzői. A beteg bőrszíne rózsaszín, mellkasa is hordó alakú, a nyakon vénák duzzadnak, az étvágycsökkenés miatt a testsúly csökken, és megközelítheti a veszélyes értékek határát.
- A fő tünet a légszomj, amely nyugalomban is megfigyelhető.
- A fertőzések ritkák, mert a tüdő még mindig megbirkózik a szűréssel.
- A "cor pulmonale" típusú deformáció ritka, az oxigénhiány nem olyan kifejezett.
- röntgen. A képen a szív bullái és deformitása látható.
- Diffúz képesség - nyilvánvalóan jelentősen csökkent.
- Előrejelzés. A statisztikák szerint ennek a típusnak hosszabb a várható élettartama.
A tüdőtágulásos típust népies nevén „rózsaszín puffannak” is nevezik, és ez eléggé pontos is: az ilyen hodl-típusú beteg általában vékony, természetellenesen rózsaszín bőrszínű, állandóan fulladoz, és inkább ki sem hagyja a házat.
Ha a páciens mindkét típusra utal, vegyes COPD-fenotípusról beszél – ez meglehetősen gyakran, változatos változatokban fordul elő. Az elmúlt években a tudósok több altípust is azonosítottak:
- gyakori exacerbációkkal. Akkor van beállítva, ha a beteget évente legalább négy alkalommal exacerbációkkal kórházba küldik. A C és D szakaszban fordul elő.
- Bronchiális asztmával. Az esetek harmadában fordul elő - a COPD összes tünetével a beteg megkönnyebbülést tapasztal, ha gyógyszereket használ az asztma leküzdésére. Asztmás rohamai is vannak.
- Korai kezdés. Gyors fejlődés jellemzi, és genetikai hajlam magyarázza.
- Fiatal korban. A COPD az idősek betegsége, de fiatalabbakat is érinthet. Ebben az esetben általában sokszor veszélyesebb, és magas a halálozási aránya.
Egyidejű betegségek
 A COPD-vel a páciensnek nagy eséllyel szenved nemcsak magától az elzáródástól, hanem az azt kísérő betegségektől is. Közöttük:
A COPD-vel a páciensnek nagy eséllyel szenved nemcsak magától az elzáródástól, hanem az azt kísérő betegségektől is. Közöttük:
- Szív- és érrendszeri betegségek, a szívkoszorúér-betegségtől a szívelégtelenségig. Az esetek csaknem felében fordulnak elő, és nagyon egyszerűen magyarázzák: a szervezet oxigénhiányával a szív- és érrendszer nagy stresszt tapasztal: a szív gyorsabban mozog, a vér gyorsabban áramlik a vénákon, az erek lumenje szűkül. Egy idő után a páciens mellkasi fájdalmakat, ingadozó pulzust, fejfájást és fokozott légszomjat észlel. Azon betegek harmada, akiknél a COPD-t szív- és érrendszeri betegségek kísérik, belehal.
- Csontritkulás. Az esetek harmadában fordul elő. Nem végzetes, de nagyon kellemetlen és oxigénhiány is provokálja. Fő tünete a csontok törékenysége. Ennek eredményeként a beteg gerince meggörbül, a testtartás romlik, a hát és a végtagok fájnak, éjszakai görcsök a lábakban és általános gyengeség figyelhető meg. Csökkent állóképesség, ujjmozgás. Bármely törés nagyon hosszú ideig gyógyul, és végzetes is lehet. Gyakran vannak problémák a gyomor-bél traktusban - székrekedés és hasmenés, amelyeket az ívelt gerinc nyomása okoz a belső szervekre.
- Depresszió. A betegek közel felében fordul elő. Veszélyeit gyakran alábecsülik, miközben a beteg tónus-, energia- és motivációhiánytól, öngyilkossági gondolatoktól, fokozott szorongástól, magányérzéstől és tanulási problémáktól szenved. Minden komor fényben látszik, a hangulat folyamatosan nyomott. Ennek oka egyrészt az oxigénhiány, másrészt a COPD-nek a beteg életére gyakorolt hatása. A depresszió nem végzetes, de nehezen kezelhető, és jelentősen csökkenti az élet örömét, amelyet a beteg kaphat.
- Fertőzések. A betegek hetven százalékában fordulnak elő, és az esetek harmadában halált okoznak. Ez azzal magyarázható, hogy a COPD által érintett tüdők nagyon érzékenyek bármilyen kórokozóra, és nehéz eltávolítani bennük a gyulladást. Ezenkívül a köpettermelés növekedése a légáramlás csökkenését és a légzési elégtelenség kockázatát jelenti.
- Alvási apnoe szindróma. Apnoe esetén a beteg éjszaka több mint tíz másodpercre leáll a légzése. Emiatt állandó oxigén éhezésben szenved, és akár légzési elégtelenségbe is belehalhat.
- Folyami rák. Gyakran előfordul, és ötből egy esetben halált okoz. Ez a fertőzésekhez hasonlóan a tüdő sebezhetőségével magyarázható.
A férfiaknál a COPD-t gyakran impotencia kíséri, időseknél pedig szürkehályogot okoz.
Diagnózis és rokkantság
 A COPD diagnózisának megfogalmazása egy egész képletet foglal magában, amelyet az orvosok követnek:
A COPD diagnózisának megfogalmazása egy egész képletet foglal magában, amelyet az orvosok követnek:
- a betegség neve krónikus tüdőbetegség;
- COPD fenotípus - vegyes, hörghurut, emphysematous;
- a bronchiális obstrukció súlyossága - enyhétől a rendkívül súlyosig;
- a COPD-tünetek súlyossága - CAT határozza meg;
- az exacerbációk gyakorisága - kettőnél több gyakori, kevésbé ritka;
- kísérő betegségek.
Ennek eredményeként a tervnek megfelelő vizsgálatot követően a beteg diagnózist kap, amely például így hangzik: „krónikus obstruktív tüdőbetegség, bronchitis típusú, II. fokú hörgőelzáródás súlyos tünetekkel, gyakori exacerbációkkal, súlyosbítja a csontritkulás.”
A vizsgálat eredménye alapján kezelési tervet készítenek, és a beteg fogyatékosság megállapítását kérheti - minél súlyosabb a COPD, annál valószínűbb, hogy az első csoport megszületik.
És bár a COPD-t nem kezelik, a betegnek minden tőle telhetőt meg kell tennie annak érdekében, hogy egy bizonyos szinten megőrizze egészségét – és akkor életének minősége és időtartama egyaránt nő. A legfontosabb dolog az, hogy optimista legyen a folyamat során, és ne hagyja figyelmen kívül az orvosok tanácsait.
5
1 FGBOU VO RNIMU őket. N.I. Pirogov, Oroszország Egészségügyi Minisztériuma, Moszkva
2 Pulmonológiai Kutatóintézet, Oroszország Szövetségi Orvosi és Biológiai Ügynöksége, Moszkva
3 Szövetségi Állami Költségvetési Felsőoktatási Intézmény, Oroszország Egészségügyi Minisztériumának USMU, Jekatyerinburg
4 FGAOU VO Első Moszkvai Állami Orvostudományi Egyetem. I. M. Sechenov, Oroszország Egészségügyi Minisztériuma (Sechenov Egyetem), Moszkva
5 FGBNU "TsNIIT", Moszkva
Idézethez: Chuchalin A.G., Aisanov Z.R., Avdeev S.N., Leshchenko I.V., Ovcharenko S.I., Shmelev E.I. Szövetségi klinikai irányelvek a krónikus obstruktív tüdőbetegség diagnosztizálására és kezelésére // BC. 2014. 5. sz. S. 331
1. Módszertan
1. Módszertan
A bizonyítékok gyűjtésére/kiválasztására használt módszerek:
. keresés elektronikus adatbázisokban.
A bizonyítékok összegyűjtésére/kiválasztására használt módszerek leírása:
. Az ajánlások bizonyítéka a Cochrane Library, az EMBASE és a MEDLINE adatbázisokban található publikációk. A keresés mélysége 5 év volt.
A bizonyítékok minőségének és erősségének értékelésére használt módszerek:
. szakértői konszenzus;
. a szignifikancia értékelése a minősítési rendszer szerint (1. táblázat).
A bizonyítékok elemzésére használt módszerek:
. publikált metaanalízisek áttekintése;
. szisztematikus áttekintések bizonyítéktáblázatokkal.
A bizonyítékok elemzéséhez használt módszerek leírása.
A publikációk potenciális bizonyítékforrásként történő kiválasztásakor az egyes tanulmányokban alkalmazott módszertanokat felülvizsgálják annak érvényessége érdekében. A vizsgálat eredménye befolyásolja a publikációhoz rendelt bizonyítékok szintjét, ami viszont befolyásolja az abból következő ajánlások erősségét.
A módszertani vizsgálat több kulcskérdésre épül, amelyek a vizsgálati terv azon sajátosságaira összpontosítanak, amelyek jelentős hatással vannak az eredmények és a következtetések érvényességére. Ezek a kulcskérdések a tanulmányok típusától és a publikáció-értékelési folyamat szabványosítására használt kérdőívektől függően változhatnak. Az ajánlások az Új-Dél-Wales Egészségügyi Minisztériuma által kidolgozott MERGE kérdőívet használták. Ezt a kérdőívet az Orosz Légzőgyógyászati Társaság követelményeinek megfelelő részletes értékelésre és adaptálásra szánjuk a módszertani szigor és a gyakorlati alkalmazás lehetősége közötti optimális egyensúly fenntartása érdekében.
Az értékelési folyamatot természetesen a szubjektív tényező is befolyásolhatja. A lehetséges hibák minimalizálása érdekében minden tanulmányt egymástól függetlenül, azaz a munkacsoport legalább két független tagja értékelt. Az értékelési különbségeket már az egész csoport megvitatta. Ha nem sikerült konszenzusra jutni, független szakértőt vontak be.
Bizonyítéktáblázatok:
. a bizonyítéktáblázatokat a munkacsoport tagjai töltötték ki.
Az ajánlások megfogalmazására használt módszerek:
. szakértői konszenzus.
Főbb ajánlások:
Az ajánlások bemutatásakor megadásra kerül az ajánlások erőssége (A-D), a bizonyítékok szintje (1++, 1+, 1-, 2++, 2+, 2-, 3, 4) és a helyes gyakorlat mutatói (jó gyakorlati pontok). az ajánlások szövege (1. táblázat) 1. és 2.).
2. A krónikus obstruktív tüdőbetegség (COPD) meghatározása és epidemiológiája
Meghatározás:
A COPD egy olyan betegség, amelyet részlegesen visszafordítható obstruktív lélegeztetési zavar jellemez, amely rendszerint progresszív, és a tüdő megnövekedett krónikus gyulladásos válaszával jár a patogén részecskék vagy gázok hatására. Egyes betegeknél az exacerbációk és társbetegségek befolyásolhatják a COPD általános súlyosságát.
Hagyományosan a COPD kombinálja a krónikus bronchitist és a tüdőtágulatot.
A krónikus hörghurut klinikailag általában legalább 3 hónapig tartó köhögés és köpet termelést jelent. a következő 2 évben. Az emfizémát morfológiailag úgy határozzák meg, mint a légutak állandó tágulását a terminális hörgőktől távolabb, az alveoláris falak pusztulásával, és nem jár együtt fibrózissal. COPD-s betegeknél mindkét állapot leggyakrabban jelen van, és nehéz őket klinikailag megkülönböztetni.
A COPD fogalma nem foglalja magában a bronchiális asztmát (BA) és más, rosszul reverzibilis hörgőelzáródással járó betegségeket (cisztás fibrózis, bronchiectasia, bronchiolitis obliterans).
Járványtan
Prevalencia
A COPD jelenleg globális probléma. A világ egyes részein a COPD prevalenciája nagyon magas (Chilében több mint 20%), másutt kevesebb (Mexikóban kb. 6%). Ennek az eltérésnek az okai az emberek életmódjában, viselkedésében és a különféle károsítókkal való érintkezésben mutatkozó különbségek.
Az egyik globális tanulmány (a BOLD projekt) egyedülálló lehetőséget kínált a COPD prevalenciájának becslésére szabványosított kérdőívek és tüdőfunkciós tesztek segítségével 40 év feletti felnőtt populációban a fejlett és a fejlődő országokban egyaránt. A COPD II. és magasabb stádiumú (GOLD 2008) prevalenciája a BOLD vizsgálat szerint a 40 év felettiek körében 10,1±4,8%, ebből a férfiaknál 11,8±7,9%, a nőknél pedig 8,5±5,8%. A COPD prevalenciájáról szóló epidemiológiai tanulmány szerint a szamarai régióban (30 éves és idősebb lakosok) a COPD prevalenciája a teljes mintában 14,5% volt (a férfiak körében - 18,7%, a nők körében - 11,2%). Egy másik, az Irkutszk régióban végzett orosz tanulmány eredményei szerint a COPD prevalenciája a 18 év felettieknél a városi lakosság körében 3,1%, a vidéki lakosság körében 6,6%. A COPD prevalenciája az életkor előrehaladtával nőtt: az 50-69 éves korcsoportban a városban a férfiak 10,1%-a, a vidéki területeken pedig 22,6%-a szenvedett a betegségben. Szinte minden második vidéki 70 év feletti férfinél diagnosztizáltak COPD-t.
Halálozás
A WHO szerint a COPD jelenleg a 4. vezető halálok a világon. Évente körülbelül 2,75 millió ember hal meg COPD-ben, ami az összes halálozási ok 4,8%-a. Európában a COPD halálozási aránya jelentős eltéréseket mutat: Görögországban, Svédországban, Izlandon és Norvégiában 0,2/100 ezer lakos, Ukrajnában és Romániában 80/100 ezer.
1990 és 2000 között a szív- és érrendszeri betegségek (CVD) halálozása általában 19,9%-kal, illetve 6,9%-kal csökkent, míg a COPD-halálozás 25,5%-kal nőtt. A COPD okozta halálozás különösen kifejezett növekedése a nők körében figyelhető meg.
A COPD-s betegek mortalitásának előrejelzői olyan tényezők, mint a hörgőelzáródás súlyossága, a tápláltsági állapot (testtömegindex (BMI)), a fizikai állóképesség a 6 perces séta teszt alapján és a nehézlégzés súlyossága, az exacerbációk gyakorisága és súlyossága. , pulmonális hipertónia.
A COPD-s betegek halálozásának fő okai a légzési elégtelenség (RF), a tüdőrák, a szív- és érrendszeri betegségek és más lokalizációjú daganatok.
A COPD társadalmi-gazdasági jelentősége
A fejlett országokban a COPD-vel összefüggő összes gazdasági költség a tüdőbetegségek szerkezetében a tüdőrák után a 2., a közvetlen költségek tekintetében pedig az 1. helyet foglalja el, 1,9-szeresével haladva meg a BA közvetlen költségeit. A COPD-vel összefüggő egy betegre jutó gazdasági költségek háromszor magasabbak, mint az egy asztmás betegre jutó költségek. A COPD-ben a közvetlen orvosi költségekről szóló néhány jelentés azt jelzi, hogy az anyagi források több mint 80%-a a betegek fekvőbeteg-ellátására, és kevesebb mint 20%-aa járóbeteg-ellátásra irányul. Megállapítást nyert, hogy a költségek 73%-a a súlyos betegségben szenvedő betegek 10%-át terheli. A legnagyobb gazdasági kárt a COPD exacerbációinak kezelése okozza. Oroszországban a COPD gazdasági terhe, figyelembe véve a közvetett költségeket, beleértve a hiányzást (hiányzás) és a prezentációt (rossz egészségi állapot miatt kevésbé hatékony munka), 24,1 milliárd rubel.
3. A COPD klinikai képe
A kockázati tényezőknek való kitettség körülményei között (aktív és passzív dohányzás, exogén szennyező anyagok, bioorganikus tüzelőanyagok stb.) a COPD általában lassan fejlődik ki és fokozatosan halad előre. A klinikai kép sajátossága, hogy a betegség hosszú ideig kifejezett klinikai megnyilvánulások nélkül halad (3, 4; D).
Az első jele annak, hogy a betegek orvoshoz fordulnak, a köhögés, gyakran köpet termeléssel és/vagy légszomj. Ezek a tünetek a legkifejezettebbek reggel. A hideg évszakokban "gyakori megfázás" fordul elő. Ez a betegség kezdetének klinikai képe.
A krónikus köhögést - általában a COPD első tünetét - gyakran alábecsülik a betegek és az orvosok, mivel azt a dohányzás és/vagy a káros környezeti tényezőknek való kitettség várható következményének tekintik. Általában a betegek kis mennyiségű viszkózus köpet termelnek. A köhögés és a köpettermelés fokozódása leggyakrabban a téli hónapokban, a fertőzéses exacerbációk idején fordul elő.
A légszomj a COPD legfontosabb tünete (4; D). Ez gyakran indok az orvosi segítség kérésére, és a fő ok, amely korlátozza a beteg munkatevékenységét. A nehézlégzés egészségügyi hatását a British Medical Research Council (mMRC) kérdőív segítségével értékelik. Kezdetben a légszomjat viszonylag magas szintű fizikai aktivitás esetén észlelik - például sík terepen futva vagy lépcsőn sétálva. A betegség előrehaladtával a dyspnoe súlyosbodik, és korlátozhatja a napi aktivitást is, később pedig nyugalomban jelentkezik, így a beteg otthon marad (3. táblázat). Ezenkívül a nehézlégzés mMRC skálán történő értékelése érzékeny eszköz a COPD-s betegek túlélési előrejelzésére.
A COPD-klinika leírásánál figyelembe kell venni az adott betegségre jellemző sajátosságokat: szubklinikai megjelenését, specifikus tünetek hiányát és a betegség egyenletes előrehaladását.
A tünetek súlyossága a betegség lefolyásának szakaszától függően változik (stabil lefolyás vagy súlyosbodás). Stabilnak azt az állapotot kell tekinteni, amikor a tünetek súlyossága hetekig, akár hónapokig nem változik jelentősen, és ebben az esetben a betegség előrehaladása csak hosszú távú (6-12 hónapos) dinamikus monitorozással mutatható ki. beteg.
A betegség súlyosbodása különös hatással van a klinikai képre - az állapot visszatérő (legalább 2-3 napig tartó) romlása, amelyet a tünetek és a funkcionális zavarok intenzitásának növekedése kísér. Az exacerbáció során fokozódik a hiperinfláció és az úgynevezett „levegőcsapdák” súlyossága a kilégzési áramlás csökkenésével kombinálva, ami fokozott nehézlégzéshez vezet, amit általában távoli sípoló légzés megjelenése vagy felerősödése kísér. nyomás érzete a mellkasban, és csökken az edzéstűrő képesség. Ezenkívül nő a köhögés intenzitása, a köpet mennyisége, elválasztásának jellege, a szín és a viszkozitás megváltozik (élesen nő vagy csökken). Ugyanakkor a külső légzésfunkció (RF) és a vérgázok mutatói romlanak: csökkennek a sebességjelzők (1 s alatti kényszerkilégzési térfogat (FEV1) stb.), hipoxémia, sőt hypercapnia is előfordulhat. Az exacerbációk fokozatosan, fokozatosan kezdődhetnek, vagy a beteg állapotának gyors romlásával jellemezhetők akut légzési elégtelenség, ritkábban jobb kamrai elégtelenség kialakulásával.
A COPD lefolyása egy stabil fázis és a betegség súlyosbodásának váltakozása, de különböző embereknél eltérően megy végbe. A COPD progressziója azonban gyakori, különösen akkor, ha a beteg továbbra is ki van téve a belélegzett patogén részecskéknek vagy gázoknak. A betegség klinikai képe is komolyan függ a betegség fenotípusától, és fordítva, a fenotípus határozza meg a COPD klinikai megnyilvánulásainak jellemzőit. Hosszú évek óta a betegek emphysematous és bronchitis fenotípusokra oszthatók.
A bronchitis típusát a bronchitis (köhögés, köpet) jeleinek túlsúlya jellemzi. Az emfizéma ebben az esetben kevésbé kifejezett. A tüdőtágulásos típusban éppen ellenkezőleg, a tüdőtágulás a vezető kóros megnyilvánulás, a légszomj uralkodik a köhögés felett. A klinikai gyakorlatban azonban nagyon ritkán lehet megkülönböztetni a COPD emphysematous vagy bronchitis fenotípusát az úgynevezett "tiszta" formában (helyesebb lenne a betegség túlnyomórészt bronchitises vagy túlnyomóan emphysemás fenotípusáról beszélni). A fenotípusok jellemzőit részletesebben a 4. táblázat mutatja be.
Ha lehetetlen kiemelni egyik vagy másik fenotípus túlsúlyát, vegyes fenotípusról kell beszélni. Klinikai körülmények között gyakoribbak a vegyes típusú betegségben szenvedő betegek.
A fentieken kívül jelenleg a betegség más fenotípusait is megkülönböztetik. Ez mindenekelőtt az úgynevezett átfedési fenotípusra vonatkozik (COPD és BA kombinációja). Gondosan meg kell különböztetni a COPD-s és asztmás betegeket. De annak ellenére, hogy ezekben a betegségekben jelentős különbségek vannak a krónikus gyulladásban, egyes betegeknél a COPD és az asztma egyidejűleg is jelen lehet. Ez a fenotípus kialakulhat asztmás dohányosoknál. Ezzel párhuzamosan nagyszabású vizsgálatok eredményeként kimutatták, hogy a COPD-s betegek mintegy 20-30%-ánál előfordulhat reverzibilis hörgőelzáródás, gyulladás során eozinofilek jelennek meg a sejtösszetételben. Ezen betegek egy része a COPD + BA fenotípusnak is tulajdonítható. Ezek a betegek jól reagálnak a kortikoszteroid-kezelésre.
Egy másik, a közelmúltban tárgyalt fenotípus a gyakori exacerbációban szenvedő betegek (évente 2 vagy több exacerbáció vagy 1 vagy több exacerbáció, amely kórházi kezelést eredményez). Ennek a fenotípusnak a jelentőségét az határozza meg, hogy a beteg az exacerbációból a tüdő funkcionális paramétereinek csökkenése mellett kerül ki, és az exacerbációk gyakorisága közvetlenül befolyásolja a betegek várható élettartamát, ezért a kezelés egyéni megközelítése szükséges. Számos további fenotípus azonosítása további tisztázást igényel. A közelmúltban számos tanulmány hívta fel a figyelmet a COPD klinikai megnyilvánulásai közötti különbségekre a férfiak és a nők között. Mint kiderült, a nőket a légutak kifejezettebb hiperreaktivitása jellemzi, kifejezettebb légszomjat észlelnek ugyanolyan szintű hörgőelzáródás mellett, mint a férfiaknál stb. Ugyanazon funkcionális mutatókkal a nők oxigénellátása jobb, mint a férfiaknál. férfiak. A nők azonban nagyobb valószínűséggel alakulnak ki exacerbációkban, a rehabilitációs programokban kevésbé mutatják be a fizikai edzés hatását, és életminőségüket (QoL) alacsonyabbra értékelik a standard kérdőívek alapján.
Köztudott, hogy a COPD-ben szenvedő betegeknél a betegség számos extrapulmonális megnyilvánulása van a COPD-ben rejlő krónikus gyulladás szisztémás hatása miatt. Ez mindenekelőtt a perifériás vázizmok működési zavaraira vonatkozik, ami jelentősen hozzájárul a terheléstűrő képesség csökkenéséhez. A krónikus, tartós gyulladás fontos szerepet játszik a vaszkuláris endotélium károsodásában és az érelmeszesedés kialakulásában COPD-s betegeknél, ami viszont hozzájárul a szív- és érrendszeri betegségek (arteriális hipertónia (AH), szívkoszorúér-betegség (CHD), akut miokardiális infarktus AMI), szívelégtelenség (HF) ) COPD-s betegeknél, és növeli a halálozás kockázatát. A táplálkozási állapot változása egyértelműen megnyilvánul. A csökkent tápláltsági állapot viszont önálló kockázati tényezőként szolgálhat a betegek halálához. A szisztémás gyulladás szintén hozzájárul a csontritkulás kialakulásához. A COPD-ben szenvedő betegeknél kifejezettebbek a csontritkulás jelei, mint a COPD-ben nem szenvedő betegek azonos korcsoportjában. A közelmúltban felhívják a figyelmet arra, hogy a policitémia mellett a COPD-s betegek 10-20%-ában vérszegénység fordul elő. Ennek oka nem teljesen ismert, de okkal feltételezhető, hogy a krónikus gyulladás szisztémás hatásának következménye a COPD-ben.
A betegség klinikai képére jelentős hatást gyakorolnak a neuropszichiátriai rendellenességek, amelyek memóriavesztésben, depresszióban, „félelmek” megjelenésében és alvászavarban nyilvánulnak meg.
A COPD-s betegekre jellemző a kísérő betegségek gyakori kialakulása, amelyek idős betegeknél fordulnak elő, függetlenül a COPD jelenlététől, de jelenléte esetén - nagyobb valószínűséggel (CHD, magas vérnyomás, alsó végtagok érrendszeri érelmeszesedése stb.) . Más társbetegségek (diabetes mellitus (DM), gastrooesophagealis reflux betegség, BPH, ízületi gyulladás) együtt létezhetnek a COPD-vel, mivel ezek az öregedési folyamat részét képezik, és szintén jelentős hatással vannak a COPD-s betegek klinikai képére.
A COPD természetes kialakulásának folyamatában a klinikai kép megváltozhat a betegség kialakuló szövődményeinek figyelembevételével: tüdőgyulladás, pneumothorax, akut DN (ARN), tüdőembólia (PE), bronchiectasia, tüdővérzés, cor pulmonale, ill. dekompenzációja súlyos keringési elégtelenséggel.
Összefoglalva a klinikai kép leírását, hangsúlyozni kell, hogy a betegség klinikai megnyilvánulásainak súlyossága a fenti tényezők közül soktól függ. Mindez, valamint a kockázati tényezőknek való kitettség intenzitása, a betegség progressziójának üteme a páciens megjelenését kelti életének különböző időszakaiban.
4. A diagnózis alapelvei
A COPD helyes diagnosztizálásához mindenekelőtt a betegség definíciójából fakadó legfontosabb (alap) rendelkezésekre kell támaszkodni. A COPD diagnózisát minden köhögésben, köpettermelésben vagy nehézlégzésben szenvedő betegnél mérlegelni kell, és azonosítani kell a COPD kockázati tényezőit. A való életben, a betegség korai szakaszában a dohányos nem tartja magát betegnek, mert a köhögést normális állapotnak értékeli, ha a munkatevékenységét még nem zavarták. Még a fizikai megerőltetés során fellépő légszomj megjelenését is az öregség vagy az edzés következtében fellépő következményeknek tekinti.
A COPD diagnózisának felállítását segítő kulcsfontosságú anamnesztikus tényező a kórokozók, elsősorban a dohányfüst légzőszerveinek inhalációs expozíciója tényének megállapítása. A dohányzási státusz értékelésekor mindig feltüntetjük a dohányzó személyek indexét (csomagévek). Az anamnézis gyűjtése során nagy figyelmet kell fordítani a passzív dohányzás epizódjainak azonosítására is. Ez minden korcsoportra vonatkozik, beleértve a magzati dohányfüstnek való kitettséget a méhen belül, ami a terhes nő vagy a körülötte lévők általi dohányzás eredménye. A foglalkozási inhalációs expozíció a dohányzással együtt a COPD kialakulását elősegítő tényezőnek tekinthető. Ez vonatkozik a munkahelyi légszennyezés különböző formáira, beleértve a gázokat és aeroszolokat, valamint a fosszilis tüzelőanyagokból származó füstnek való kitettséget.
Ezért a COPD diagnózisának a következő területeket kell magában foglalnia:
- kockázati tényezők azonosítása;
- az elzáródás tüneteinek tárgyiasítása;
- a tüdő légzésfunkciójának monitorozása.
Ebből következik, hogy a COPD diagnózisa több szakasz elemzésén alapul:
- verbális portré készítése a páciensről a vele folytatott beszélgetésből nyert információk alapján (gondos anamnézis gyűjtése);
- objektív (fizikai) vizsgálat;
- laboratóriumi és műszeres vizsgálatok eredményei. A COPD diagnózisát mindig spirometriával kell megerősíteni. Bronchodilatáció utáni FEV1 értékek / kényszerített vitálkapacitás (FVC)<70% - обязательный признак ХОБЛ, который существует на всех стадиях заболевания.
Tekintettel arra, hogy a COPD-nek nincsenek specifikus megnyilvánulásai, és a diagnózis kritériuma egy spirometrikus indikátor, a betegség hosszú ideig diagnosztizálatlan maradhat. Az aluldiagnosztizáltság problémája összefügg azzal is, hogy a COPD-ben szenvedők közül sokan nem érzik rosszul magukat a légszomj hiánya miatt a betegség kialakulásának egy bizonyos szakaszában, és nem kerülnek az orvos látóterébe. Ebből következik, hogy az esetek túlnyomó többségében a COPD-t a betegség rokkantsági szakaszában diagnosztizálják.
Az egyes dohányzó betegekkel folytatott részletes beszélgetés hozzájárul a betegség korai felismeréséhez, hiszen aktív kérdezősködéssel, panaszok hiányával azonosíthatók a hörgőfán a krónikus gyulladás kialakulására jellemző jelek, elsősorban a köhögés.
A pácienssel folytatott beszélgetés során használhatja a kérdőívet a COPD* diagnosztizálására (5. táblázat).
A bronchiális fa és a tüdő parenchyma visszafordíthatatlan változásainak kialakulása során légszomj jelentkezik (a pácienssel folytatott beszélgetés során fel kell mérni annak súlyosságát, a fizikai aktivitással való összefüggést stb.).
A betegség korai stádiumában (ha valamilyen okból a beteg ekkor még az orvos figyelmébe kerül) a vizsgálat nem tár fel COPD-re jellemző eltérést, de a klinikai tünetek hiánya sem zárja ki jelenlétét. Az emfizéma növekedésével és a hörgőelzáródás visszafordíthatatlan összetevőjével a kilégzés szorosan zárt vagy összehajtott ajkakon keresztül történhet, ami a kis hörgők kifejezett kilégzési összeomlását jelzi, és lelassítja a kilélegzett levegő áramlási sebességét, ami enyhíti a betegek állapotát. A hiperinfláció egyéb jelei lehetnek a hordó alakú mellkas, a bordák vízszintes iránya, a szív tompaságának csökkenése.
A Scalenae és a Sternocleidomastoideus izomzat bevonása a légzésbe a légzési mechanika megsértésének további súlyosbodását és a légzőkészülék terhelésének növekedését jelzi. Egy másik jel lehet a hasüreg elülső falának paradox mozgása - annak visszahúzódása az inspiráció során, ami a rekeszizom fáradtságát jelzi. A membrán ellaposodása az alsó bordák visszahúzódásához vezet a belégzés során (Hoover-jel), és a kyphosternalis szög kiszélesedéséhez vezet. A légzőizmok fáradtságával gyakran hypercapnia lép fel, amely megfelelő értékelést igényel.
A betegek fizikális vizsgálata során száraz sípoló hangok meghallgatásával tárgyiasítható a hörgőelzáródás, ütőhangszerek során pedig dobozos ütőhang igazolja a hiperinfláció jelenlétét.
A laboratóriumi diagnosztikai módszerek közül a kötelező vizsgálatok közé tartozik a klinikai vérvizsgálat és a köpet citológiai vizsgálata. Súlyos emfizéma és fiatal beteg esetén az α1-antitripszint meg kell határozni. A betegség súlyosbodásával a leggyakrabban a neutrofil leukocitózis fordul elő szúrással és az ESR növekedésével. A leukocitózis jelenléte további érvként szolgál egy fertőző tényező mellett, amely a COPD súlyosbodásának oka. Mind a vérszegénység (egy általános gyulladásos szindróma eredménye), mind a policitémia kimutatható. Policitémiás szindróma (a vörösvértestek számának növekedése, magas hemoglobinszint)
>16 g/dl nőknél és >18 g/dl férfiaknál, a hematokrit >47%-os növekedése nőknél és >52% férfiaknál) súlyos és elhúzódó hypoxemia fennállását jelezheti.
A köpet citológiai vizsgálata információt nyújt a gyulladásos folyamat természetéről és súlyosságáról. Az atipikus sejtek meghatározása növeli az onkológiai éberséget, és további vizsgálati módszerek alkalmazását igényli.
A köpet kulturális mikrobiológiai vizsgálatát a fertőző folyamat ellenőrizetlen progressziójával kell elvégezni, és a racionális antibiotikum-terápia kiválasztására kell használni. Ugyanebből a célból a bronchoszkópia során kapott hörgőtartalom bakteriológiai vizsgálatát végzik.
Minden COPD-gyanús betegnél mellkasröntgenet kell végezni. Ez a módszer nem érzékeny eszköz a diagnózis felállítására, de lehetővé teszi a hasonló klinikai tünetekkel járó egyéb betegségek (tumor, tuberkulózis, pangásos szívelégtelenség stb.) kizárását, valamint az exacerbáció időszakában - tüdőgyulladás, pleurális folyadékgyülem kimutatását. , spontán pneumothorax stb. Ezen kívül a bronchiális obstrukció alábbi radiológiai jelei azonosíthatók: a kupola ellaposodása és a rekeszizom mozgékonyságának korlátozása légzési mozgások során, a mellkasi üreg elülső-hátul méretének változása, a retrosternalis tér kitágulása , a szív függőleges elhelyezkedése.
A bronchoszkópos vizsgálat további módszerként szolgál a COPD diagnosztizálására, hogy kizárjon más, hasonló tünetekkel járó betegségeket és állapotokat.
Az elektrokardiográfiát és az echokardiográfiát a légúti tünetek kardiális eredetének kizárására és a jobb szív hipertrófiájára utaló jelek azonosítására végezzük.
Minden COPD-re gyanús betegnek spirometriát kell végeznie.
5. Funkcionális diagnosztikai vizsgálatok
a COPD lefolyásának nyomon követése
A spirometria a fő módszer a tüdőfunkció változásainak diagnosztizálására és dokumentálására COPD-ben. A spirometriás mutatók alapján felépítettük a COPD osztályozását az obstruktív lélegeztetési zavarok súlyossága szerint. Lehetővé teszi más, hasonló tünetekkel járó betegségek kizárását.
A spirometria az előnyben részesített kezdeti vizsgálat a légúti obstrukció jelenlétének és súlyosságának felmérésére.
Módszertan
. Különféle ajánlások léteznek a spirometria alkalmazására az obstruktív tüdőbetegség diagnosztizálására és súlyosságának meghatározására.
. A tüdőfunkció kényszerspirometriás módszerrel történő vizsgálata 3 műszakilag elfogadható légzési manőver elérése esetén tekinthető befejezettnek. Ugyanakkor az eredményeknek reprodukálhatónak kell lenniük: a maximális és a következő FVC-mutatók, valamint a maximális és az azt követő FEV1-mutatók legfeljebb 150 ml-rel térhetnek el egymástól. Azokban az esetekben, amikor az FVC-érték nem haladja meg az 1000 ml-t, az FVC és a FEV1 maximális megengedett eltérése nem haladhatja meg a 100 ml-t.
. Ha 3 kísérlet után nem kap reprodukálható eredményeket, a légzési manővereket 8 kísérletig kell folytatni. A több légzési manőver a beteg fáradtságához és ritka esetekben a FEV1 vagy FVC csökkenéséhez vezethet.
. Ha ismételt kényszermanőverek hatására az értékek 20%-nál nagyobb mértékben esnek a kezdeti értékhez képest, a betegbiztonság érdekében a további vizsgálatokat le kell állítani, és a mutatók dinamikáját tükrözni kell a jelentésben. A jelentésnek legalább 3 legjobb próbálkozás grafikus eredményeit és számértékeit kell bemutatnia.
. A technikailag elfogadható, de nem reprodukálható kísérletek eredményei felhasználhatók következtetés írásában, jelezve, hogy nem reprodukálhatók.
A COPD spirometriás megnyilvánulásai
A spirometria során a COPD a megnövekedett légúti ellenállás miatti kilégzési légáramlás korlátozásában nyilvánul meg (1. ábra).
A lélegeztetési zavarok obstruktív típusát a FEV1/FVC arány csökkenése jellemzi<0,7.
Az áramlás-térfogat görbe kilégzési részének bemélyedése van, lefelé tartó térde homorú alakot ölt. A linearitás elvesztése az áramlás-térfogat görbe alsó felében az obstruktív lélegeztetési zavarok jellemzője, még akkor is, ha a FEV1/FVC arány >0,7. A változások súlyossága az obstruktív rendellenességek súlyosságától függ.
A bronchiális obstrukció előrehaladtával a kilégzési áramlás tovább csökken, a "levegőcsapdák" növekedése és a tüdő hiperinflációja az FVC csökkenéséhez vezet. A vegyes obstruktív-restrikciós rendellenességek kizárása érdekében testpletizmográfiával meg kell mérni a teljes tüdőkapacitást (TLC).
Az emphysema súlyosságának értékeléséhez meg kell vizsgálni a REL-t és a diffúziós DSL-t.
Reverzibilitási teszt (hörgőtágító teszt)
Ha a kezdeti spirometriás vizsgálat során hörgőelzáródásra utaló jeleket észlelnek, akkor célszerű reverzibilitási tesztet (hörgőtágító tesztet) végezni a hörgőtágító gyógyszerek hatására bekövetkező obstrukció reverzibilitásának mértékének megállapítása érdekében.
Az elzáródás reverzibilitásának vizsgálatára inhalációs hörgőtágítókkal végzett vizsgálatokat végeznek, értékelik ezek hatását a FEV1-re. Az áramlás-térfogat görbe egyéb mutatói, amelyek főként az FVC-ből származnak és számítanak, nem ajánlottak.
Módszertan
. A vizsgálat során rövid hatású hörgőtágítók használata javasolt a maximális egyszeri adagban:
- β2-agonisták esetében - szalbutamol 400 mcg;
- antikolinerg gyógyszerekhez - ipratropium-bromid 160 mcg.
. Egyes esetekben lehetőség van antikolinerg gyógyszerek és rövid hatású β2-agonisták kombinációjának alkalmazása a jelzett dózisokban. A kimért dózisú aeroszolos inhalátorokat távtartóval kell használni.
. 15 perc elteltével ismételt spirometriás vizsgálatot kell végezni. belélegzés után
β2-agonisták vagy 30-45 perc elteltével. antikolinerg szerek belélegzése vagy ezek kombinációja után
β2-agonisták.
A pozitív válasz kritériumai
A hörgőtágító teszt akkor tekinthető pozitívnak, ha egy hörgőtágító belélegzése után a hörgőtágulási együttható (CBD) eléri vagy meghaladja a 12%-ot, és az abszolút növekedés 200 ml vagy több:
CBD \u003d (FEV1 után (ml) - FEV1 ref. (ml) / FEV1 ref. (ml)) x 100%
Abszolút növekedés (ml) = FEV1 után (ml) - FEV1 ref. (ml)
ahol FEV1 ref. - a spirometriás indikátor értéke a hörgőtágító belégzése előtt, FEV1 után - az indikátor értéke a hörgőtágító belégzése után.
A pozitív hörgőtágító teszt megállapításához mindkét kritériumnak teljesülnie kell.
A hörgőtágító teszt értékelésekor fontos figyelembe venni a szív- és érrendszerből származó mellékhatásokat: tachycardia, aritmia, vérnyomás-emelkedés, valamint olyan tünetek megjelenése, mint az izgatottság vagy a remegés.
A spirometria eredményeinek technikai változatossága minimálisra csökkenthető a berendezés rendszeres kalibrálásával, a beteg gondos oktatásával és a személyzet képzésével.
Megfelelő értékek
A megfelelő értékek az antropometriai paraméterektől függenek, elsősorban a magasságtól, nemtől, életkortól, rassztól. Figyelembe kell azonban venni az egyéni eltéréseket is. Tehát az átlagos szint feletti kiindulási mutatókkal rendelkező embereknél a tüdőpatológia kialakulásával ezek a mutatók csökkenni fognak a kezdetiekhez képest, de továbbra is a lakossági normán belül maradhatnak.
Monitoring (soros vizsgálatok)
A spirometriás indikátorok (FEV1 és FVC) monitorozása megbízhatóan tükrözi a tüdőfunkció változásának dinamikáját a hosszú távú követés során, azonban figyelembe kell venni az eredmények technikai és biológiai változékonyságának lehetőségét.
Egészséges egyénekben az FVC és a FEV1 változása akkor tekinthető klinikailag szignifikánsnak, ha a különbség 1 napon belül ismételt vizsgálatok során meghaladja az 5%-ot, és több héten belül a 12%-ot.
A tüdőfunkció csökkenésének ütemének növekedése (több mint 40 ml/év) nem kötelező jele a COPD-nek. Ráadásul egyedileg nem igazolható, mivel a FEV1 variabilitás elfogadható szintje egy vizsgálaton belül jelentősen meghaladja ezt az értéket és 150 ml.
Kilégzési csúcsáramlás (PEF) monitorozása
A PSV-t a mutatók megnövekedett napi változékonyságának kizárására használják, amely inkább jellemző az asztmára és a gyógyszeres terápiára adott válaszreakcióra.
A legjobb mutatót a rendszer 3 kényszermanőver végrehajtási kísérlet után rögzíti, a belégzést követő legfeljebb 2 másodperc szünettel. A manővert ülve vagy állva hajtják végre. Több mérést végeznek, ha a 2 maximális PSV érték közötti különbség meghaladja a 40 l/perc értéket.
A PEF-et a légáramlás változékonyságának becslésére használják több, legalább 2 hét alatt végzett mérés során. A megnövekedett variabilitás 1 napon belül dupla méréssel rögzíthető. A gyakoribb mérések javítják a becslést. Ebben az esetben a mérési pontosság növelése különösen a csökkent együttműködési képességű betegeknél érhető el.
A PSV variabilitását legjobban a maximális és minimális értékek különbségeként lehet kiszámítani, az átlagos vagy maximális napi PSV százalékában.
A maximális indikátortól való eltérés normálértékeinek felső határa körülbelül 20%, ha 1 napon belül 4 vagy több mérést végeznek. Kettős mérés esetén azonban alacsonyabb is lehet.
A PSV variabilitása fokozható azokban a betegségekben, amelyekkel az AD leggyakrabban differenciálódik. Ezért a klinikai gyakorlatban a PSV megnövekedett variabilitásának specifikussága alacsonyabb, mint a populációs vizsgálatokban.
A PEF értékeket a klinikai helyzet figyelembevételével kell értelmezni. A PSV-vizsgálat csak a már megállapított COPD-diagnózissal rendelkező betegek monitorozására alkalmazható.
6. A COPD differenciáldiagnózisa
A COPD differenciáldiagnózisának fő feladata a hasonló tünetekkel járó betegségek kizárása. Annak ellenére, hogy a BA és a COPD között meglehetősen határozott különbségek vannak a fejlődési mechanizmusokban, a klinikai megnyilvánulásokban, valamint a megelőzés és kezelés elveiben, ennek a két betegségnek van néhány közös jellemzője. Ezenkívül ezeknek a betegségeknek a kombinációja is lehetséges egy személyben.
A BA és COPD differenciáldiagnózisa az alapvető klinikai adatok, a funkcionális és laboratóriumi vizsgálatok eredményeinek integrálásán alapul. A gyulladás jellemzőit COPD és BA esetén a 2. ábra mutatja.
E betegségek differenciáldiagnózisának vezető belépési pontjait a 6. táblázat tartalmazza.
A COPD kialakulásának bizonyos szakaszaiban, különösen a beteggel való első találkozáskor, szükségessé válik, hogy megkülönböztessük számos, hasonló tünetekkel járó betegségtől. Főbb megkülönböztető jegyeiket a 7. táblázat mutatja be.
A COPD fejlődésének különböző szakaszaiban a differenciáldiagnózis megvannak a maga sajátosságai. Az enyhe COPD-ben a legfontosabb a szubklinikailag vagy kevés tünettel járó környezeti agressziós tényezőkkel összefüggő egyéb betegségektől való eltérések azonosítása. Először is, ez a krónikus hörghurut különféle változataira vonatkozik. Súlyos COPD-ben szenvedő betegek differenciáldiagnózisának felállítása nehézségekbe ütközik. Nemcsak a beteg állapotának súlyossága, az irreverzibilis elváltozások súlyossága határozza meg, hanem a kísérő betegségek nagy halmaza is (IHD, magas vérnyomás, anyagcsere-betegségek stb.).
7. A COPD modern osztályozása.
A betegség lefolyásának súlyosságának átfogó értékelése
A COPD osztályozása (8. táblázat) az elmúlt években a tüdő funkcionális állapotának mutatói alapján, a FEV1 hörgőtágító utáni értékei alapján történt, és ebben a betegség 4 stádiumát különítették el.
A Szakértői Bizottság a GOLD 2011 programban felhagyott a „stádium” kifejezés használatával, mivel ez a mutató csak a FEV1 értéken alapul, és nem volt megfelelő a betegség súlyosságának jellemzésére. A közelmúltban végzett vizsgálatok kimutatták, hogy a stádium meghatározása nem minden esetben áll rendelkezésre a betegség esetében. Nincs bizonyíték a COPD-stádiumok valódi létezésére (az egyik szakaszból a másikba való átmenet a modern terápiával). Ugyanakkor a FEV1 értékek továbbra is relevánsak, mivel tükrözik a légáramlás-korlátozás súlyosságának mértékét (enyhe - I. stádiumtól, illetve rendkívül súlyos - IV. szakaszig). Ezeket a COPD-s betegek súlyosságának átfogó felmérésére használják.
A GOLD dokumentum 2011-es felülvizsgálata során új osztályozást javasoltak a COPD-s betegek súlyosságának integrált értékelése alapján. Nemcsak a bronchiális obstrukció súlyosságát (a hörgők átjárhatóságának mértékét) veszi figyelembe a spirometriás vizsgálat eredményei szerint, hanem a páciensre vonatkozó klinikai adatokat is: a COPD exacerbációinak évenkénti számát és a klinikai tünetek súlyosságát. az mMRC (3. táblázat) és a COPD Assessment Test (CAT) (9. táblázat) eredményei szerint.
Ismeretes, hogy a tünetek QoL-ra gyakorolt hatásának értékelésének "arany standardja" a St. George's Hospital Respiratory Questionnaire (SGRQ) eredményei, a "tünetek" skálája. A klinikai gyakorlatban szélesebb körben alkalmazzák a CAT értékelő tesztet, és újabban a Clinical COPD Questionnaire (CCQ) is.
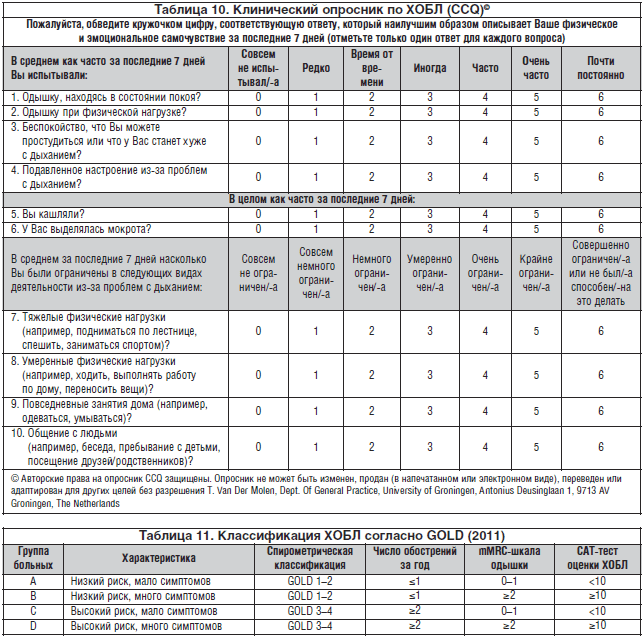
A GOLD 2013-ban a tünetek értékelése kibővült a CCQ skála alkalmazása miatt, amely lehetővé teszi mind az 1 napra, mind az utolsó hétre vonatkozóan a tünetek tárgyiasítását és nem csak minőségi, hanem klinikai jellemzőt is megadni. 10. táblázat).
A végső pontszámot az összes kérdés megválaszolásakor kapott pontszámok összegéből számítják ki, és elosztják 10-zel.<1 симптомы оцениваются как невыраженные, а при ≥1 - выраженные, т. е. оказывающие влияние на жизнь пациента. Вместе с тем еще окончательно не установлены значения CCQ, соответствующие выраженному влиянию симптомов на КЖ, эквивалентные значениям SGRQ. Пограничными значениями отличия выраженных от невыраженных симптомов предлагаются значения 1,0-1,5 (GOLD 2014).
A COPD besorolását a GOLD program ajánlásai alapján a 11. táblázat mutatja be.
A kockázat mértékének felmérésekor a GOLD légáramlási korlátnak vagy az anamnézisben előforduló exacerbációknak megfelelő legmagasabb fokozat kiválasztása javasolt.
A GOLD 2013 új kiadása egy olyan rendelkezéssel egészült ki, hogy ha a betegnek az előző évben akár csak egy exacerbációja is volt, amely kórházi kezeléshez vezetett (azaz súlyos exacerbáció), a beteget fokozottan veszélyeztetettnek kell minősíteni.
Így a COPD egy adott betegre gyakorolt hatásának integrált értékelése a tünetek és a spirometriás osztályozás értékelését kombinálja az exacerbációk kockázatának felmérésével.
A fentiek figyelembevételével a COPD diagnózisa így nézhet ki:
„Krónikus obstruktív tüdőbetegség…”, amelyet a következők értékelése követ:
- a bronchiális obstrukció súlyossága (I-IV);
- a klinikai tünetek súlyossága: súlyos (CAT ≥10, mMRC ≥2, CCQ ≥1), nem kifejezett (CAT)<10, mMRC <2, CCQ <1);
- exacerbációk gyakorisága: ritka (0-1), gyakori (≥2);
- COPD fenotípus (ha lehetséges);
- kísérő betegségek.
A kísérő betegségek szerepe rendkívül fontos a COPD súlyosságának megítélésében, azonban a legutóbbi, 2013-as GOLD ajánlásban sem kapott méltó helyet a fenti besorolásban.
8. Stabil COPD kezelése
A kezelés fő célja a betegség progressziójának megakadályozása. A kezelési célokat a 12. táblázat írja le.
A kezelés fő irányai:
I. Nem farmakológiai hatások:
- a kockázati tényezők hatásának csökkentése;
- oktatási programok.
Az expozíció nem gyógyszeres módszereit a 13. táblázat mutatja be.
Súlyos betegségben (GOLD 2-4) szenvedő betegeknél szükséges intézkedésként tüdőrehabilitációt kell alkalmazni.
II. Orvosi kezelés
A gyógyszeres terápia volumenének megválasztása a klinikai tünetek súlyosságán, a hörgőtágító utáni FEV1 értékén és a betegség exacerbációinak gyakoriságán alapul (14., 15. táblázat).
A COPD-ben szenvedő betegek farmakológiai terápiájának sémája, amelyet a COPD súlyosságának átfogó értékelésének figyelembevételével állítanak össze (a betegség súlyosbodásának gyakorisága, a klinikai tünetek súlyossága, a COPD stádiuma, a károsodott hörgők átjárhatóságának mértéke alapján) , a 16. táblázat tartalmazza.
Egyéb kezelések közé tartozik az oxigénterápia, a légzéstámogatás és a sebészeti kezelés.
Oxigénterápia
Az oxigén (O2) hosszú távú adagolása (>15 óra/nap) növeli a túlélést krónikus DN-ben és súlyos nyugalmi hipoxémiában szenvedő betegeknél (B, 2++).
Légzéstámogatás
A non-invazív lélegeztetést (NIV) széles körben alkalmazzák rendkívül súlyos, stabil lefolyású COPD-ben szenvedő betegeknél.
A NIV és a hosszú távú oxigénterápia kombinációja hatásos lehet kiválasztott betegeknél, különösen napközbeni, nyilvánvaló hypercapnia esetén.
Sebészet
Lung Volume Reduction Surgery (LUL)
A RULA-t a tüdő egy részének eltávolításával hajtják végre a hiperinfláció csökkentése és a légzőizmok hatékonyabb pumpálása érdekében. Alkalmazását felső lebeny emfizémában és alacsony terheléstűrő betegeknél végzik.
Tüdőtranszplantáció
A tüdőtranszplantáció javíthatja az életminőséget és a funkcionális teljesítményt a gondosan kiválasztott, nagyon súlyos COPD-s betegeknél. A kiválasztási kritériumok a FEV1<25% от должной величины, РаО2 <55 мм рт. ст., РаСО2 >50 Hgmm Művészet. szobalevegő belégzéskor és pulmonalis hypertonia (Pra> 40 Hgmm).
9. A COPD súlyosbodása
A COPD exacerbáció definíciója és jelentése
Az exacerbációk kialakulása a COPD lefolyásának jellegzetes jellemzője. GOLD (2013) meghatározása szerint: "A COPD exacerbációja a légúti tünetek súlyosbodásával jellemezhető akut esemény, amely meghaladja a szokásos napi ingadozásokat, és az alkalmazott terápia rendjének megváltoztatásához vezet."
A COPD súlyosbodása az egyik leggyakoribb oka annak, hogy a betegek sürgősségi orvosi ellátást kérnek. A COPD-ben szenvedő betegek exacerbációinak gyakori kialakulása a légzésfunkció és a gázcsere hosszú távú (akár több hetes) romlásához, a betegség gyorsabb progressziójához, a betegek életminőségének jelentős csökkenéséhez vezet, és összefügg a kezelés jelentős gazdasági költségei. Ezenkívül a COPD súlyosbodása az egyidejű krónikus betegségek dekompenzációjához vezet. A betegek halálának fő oka a COPD súlyos exacerbációja. Az exacerbációk kezdetétől számított első 5 napban az AMI kialakulásának kockázata több mint 2-szeresére nő.
A COPD exacerbációinak osztályozása
Az egyik legismertebb COPD exacerbáció súlyossági osztályozása, amelyet a COPD exacerbációs munkacsoport javasolt, a 17. táblázat mutatja be.
Steer et al. új skálát dolgozott ki a kórházba került COPD exacerbációban szenvedő betegek prognózisának felmérésére. A halálos kimenetel 5 legerősebb előrejelzőjét azonosították: 1) a nehézlégzés súlyossága az eMRCD skálán; 2) perifériás vér eozinopenia (<0,05 клеток x109/л); 3) признаки консолидации паренхимы легких по данным рентгенографии грудной клетки; 4) ацидоз крови (pH <7,3) и 5) мерцательная аритмия. Перечисленные признаки были объединены в шкалу DECAF (по аббревиатуре первых букв в английской транскрипции) (табл. 17).
Ez a skála kiváló megkülönböztető képességet mutatott a COPD exacerbáció során bekövetkező halál előrejelzésére.
Az exacerbációk okai
A COPD exacerbációjának leggyakoribb okai a bakteriális és vírusos légúti fertőzések, valamint a légszennyező anyagok, de az exacerbációk körülbelül 20-30%-ának okait nem lehet megállapítani.
A COPD exacerbációjában a baktériumok közül a nem tipizálható Haemophilus influenzae, a Streptococcus pneumoniae és a Moraxella catarrhalis játsszák a legnagyobb szerepet. A COPD súlyos exacerbációjában szenvedő betegek bevonásával végzett vizsgálatok kimutatták, hogy a gram-negatív enterobaktériumok és a Pseudomonas aeruginosa gyakoribbak lehetnek az ilyen betegeknél (18. táblázat).
A rinovírusok az akut légúti vírusfertőzések egyik leggyakoribb okai, és jelentős okai lehetnek a COPD exacerbációinak. Megfigyelhető, hogy a COPD súlyosbodása leggyakrabban az őszi-téli hónapokban alakul ki. A COPD exacerbációinak számának növekedése összefüggésbe hozható a légúti vírusfertőzések előfordulási gyakoriságának növekedésével a téli hónapokban, és a hideg évszakban a felső légúti hám érzékenységének növekedésével szemben.
Az exacerbációhoz hasonló és/vagy súlyosbító állapotok közé tartozik a tüdőgyulladás, a PE, a pangásos szívelégtelenség, az aritmiák, a pneumothorax és a pleurális folyadékgyülem. Ezeket az állapotokat meg kell különböztetni az exacerbációktól, és ha vannak, megfelelő kezelést kell végezni.
10. A COPD exacerbációjának kezelése
A COPD-ben szenvedő betegek kezelésének taktikáját az exacerbáció különböző fokú súlyosságával a 19. táblázat mutatja be.
Inhalációs hörgőtágítók
Az inhalációs hörgőtágítók kijelölése az egyik fő láncszem a COPD (A, 1++) exacerbációinak kezelésében. Hagyományosan a COPD exacerbációjában szenvedő betegeknek vagy gyorsan ható β2-agonistákat (szalbutamol, fenoterol) vagy gyors hatású antikolinerg szereket (ipratropium-bromid) írnak fel. A β2-agonisták és az ipratropium-bromid hatékonysága a COPD exacerbációjában megközelítőleg azonos (B, 2++), a β2-agonisták előnye a gyorsabb hatáskezdet, az antikolinerg szerek pedig - nagy biztonság és jó tolerálhatóság. Napjainkban sok szakértő a β2-agonista/ipratropium-bromid kombinációs terápiát tartja a COPD exacerbáció (B, 2++) kezelésének optimális stratégiájának, különösen a súlyos exacerbációban szenvedő COPD-s betegek kezelésében.
GKS
A COPD kórházi kezelést igénylő exacerbációiról szóló klinikai vizsgálatok szerint a szisztémás kortikoszteroidok csökkentik a remisszió kezdetéig eltelt időt, javítják a tüdőfunkciót (FEV1) és csökkentik a hipoxémiát (PaO2), valamint csökkenthetik a korai visszaesés és a kezelés sikertelenségének kockázatát, csökkentik a kezelés időtartamát. kórházi tartózkodás ideje (A, 1+). Általában 30-40 mg/nap orális prednizolon kúra javasolt 5-14 napig (B, 2++). A legfrissebb adatok szerint a szisztémás kortikoszteroidokra (C, 2+) a COPD exacerbációban szenvedő és >2%-os véreozinofíliában szenvedő betegek reagálnak a legjobban.
A szisztémás kortikoszteroidok biztonságosabb alternatívája a COPD exacerbációjában az inhalációs kortikoszteroidok, különösen a porlasztott kortikoszteroidok (B, 2++).
Antibakteriális terápia (ABT)
Mivel a baktériumok nem az összes COPD exacerbációjának okozói (50%), fontos meghatározni az ABT felírásának indikációit az exacerbációk kialakulásában. A jelenlegi irányelvek antibiotikumot ajánlanak a COPD legsúlyosabb exacerbációjában szenvedő betegek számára, például az Anthonisen I-es típusú exacerbációban (azaz fokozott légszomj, fokozott köpetmennyiség és gennyesedés esetén) vagy II-es típusú (a felsorolt 3 tünet közül kettő jelenléte) esetén. ) (B, 2++). Hasonló COPD exacerbációs forgatókönyvben szenvedő betegeknél az antibiotikumok a leghatékonyabbak, mivel az ilyen exacerbációk oka bakteriális fertőzés. Az antibiotikumok a COPD súlyos exacerbációjában szenvedő, invazív vagy NIV-t igénylő betegek számára is javasoltak (D, 3). A biomarkerek, például a C-reaktív fehérje (CRP) használata segít a COPD (C, 2+) súlyosbodásában szenvedő betegek diagnózisának és kezelésének javításában. A COPD exacerbációja során a CRP-szint ≥15 mg/l-es emelkedése a bakteriális fertőzés érzékeny jele.
A COPD exacerbációjának kezelésére legmegfelelőbb antibiotikum kiválasztása számos tényezőtől függ, mint például a COPD súlyosságától, a kezelés kedvezőtlen kimenetelének kockázati tényezőitől (pl. idősebb életkor, alacsony FEV1-értékek, korábbi gyakori exacerbációk és a korábbi antibiotikum társbetegségei). terápia (D, 3)).
A COPD enyhe és közepesen súlyos exacerbációiban kockázati tényezők nélkül modern makrolidok (azitromicin, klaritromicin), cefalosporinok (cefixim stb.) kijelölése javasolt (18. táblázat). Az amoxicillin/klavulanát vagy a légúti fluorokinolonok (levofloxacin vagy moxifloxacin) ajánlottak első vonalbeli szerekként a súlyos COPD exacerbációban és kockázati tényezőkben (B, 2++) szenvedő betegeknél. A P. aeruginosa fertőzés magas kockázata esetén ciprofloxacin és egyéb antipszeudomonális hatású gyógyszerek (B, 2++).
Oxigénterápia
A hipoxémia valós veszélyt jelent a beteg életére, ezért a COPD (B, 2++) hátterében az ARF kezelésében prioritást élvez az oxigénterápia. Az oxigénterápia célja az 55-65 Hgmm közötti PaO2 elérése. Művészet. és SaO2 88-92%. COPD-ben szenvedő betegeknél az ARF-ben leggyakrabban az orrcsapot vagy a Venturi maszkot használják az O2 szállítására. Ha az O2-t kanülön keresztül adják be, az 1-2 l/perc O2-áramlás elegendő a legtöbb beteg számára (D, 3). A Venturi maszkot tekintik az O2 bejuttatásának előnyben részesített módszerének, mivel lehetővé teszi a belélegzett keverék (FiO2) O2-frakciójának meglehetősen pontos értékét, függetlenül a páciens percnyi szellőztetésétől és belégzési áramlásától. A 24%-os FiO2 oxigénterápia átlagosan 10 Hgmm-rel növeli a PaO2-t. Art., és FiO2-vel 28% - 20 Hgmm-rel. Művészet. Az oxigénterápia megkezdése vagy megváltoztatása után a következő 30-60 percen belül. A PaCO2 és a pH (D, 3) monitorozására artériás vérgáz elemzés javasolt.
NVL
NVL - a szellőztetés előnyei mesterséges légutak beállítása nélkül. Ennek az új légzéstámogatási sorozatnak a kifejlesztése lehetővé teszi a légzőizmok biztonságos és hatékony tehermentesítését, a gázcsere helyreállítását és a nehézlégzés csökkentését ARF-ben szenvedő betegeknél. Az NIV során a beteg és a légzőkészülék közötti kapcsolatot orr- vagy arcmaszkok (ritkábban sisakok és szájrészek) használatával végzik, a beteg eszméleténél van, általában nem szükséges nyugtatók és izomlazítók használata. A NIV másik fontos előnye a gyors leállítás lehetősége, valamint szükség esetén azonnali újraindítása. Az alábbiakban felsoroljuk az NIV indikációit és ellenjavallatait.
A COPD hátterében az ARF-re vonatkozó NIV felvételi kritériumai a következők:
1. Az ARF tünetei és jelei:
- kifejezett légszomj nyugalomban;
- légzésszám >24, a segédlégzési izmok légzésében való részvétel, hasi paradoxon.
2. Károsodott gázcsere jelei:
- PaCO2 >45 Hgmm Art., pH<7,35;
- PaO2/FiO2<200 мм рт. ст.
Az ARF-re vonatkozó NIV kizárási kritériumai a következők:
1. Hagyja abba a légzést.
2. Instabil hemodinamika (hipotenzió, kontrollálatlan aritmiák vagy szívizom ischaemia).
3. A légutak védelmének képtelensége (köhögési és nyelési zavar).
4. Túlzott hörgőszekréció.
5. A tudatzavar jelei (izgatottság vagy depresszió), a beteg nem képes együttműködni az egészségügyi személyzettel.
A sürgősségi légcsőintubációt és invazív légzéstámogatást igénylő ARF-ben szenvedő betegek nem tekinthetők alkalmas jelölteknek erre a légzéstámogatási módszerre (C, 2+). A NIV az egyetlen bizonyított terápia, amely csökkentheti az ARF-ben szenvedő COPD-s betegek mortalitását (A, 1++).
Invazív légzéstámogatás
A gépi lélegeztetés olyan ARF-ben szenvedő COPD-s betegek számára javasolt, akiknél az orvosi vagy egyéb konzervatív terápia (NIV) nem vezet az állapot további javulásához (B, 2++). A lélegeztetés indikációinál nemcsak a konzervatív terápia hatásának hiányát, a funkcionális mutatók súlyosságát, hanem fejlődésük sebességét és az ARF-t okozó folyamat lehetséges visszafordíthatóságát is figyelembe kell venni.
A mechanikus lélegeztetés abszolút indikációi ARF-ben a COPD súlyosbodása hátterében:
1) légzésleállás;
2) kifejezett tudatzavarok (kábulat, kóma);
3) instabil hemodinamika (SBP<70 мм рт. ст., частота сердечных сокращений <50/мин. или >160/perc);
4) a légzőizmok fáradtsága.
A mechanikus lélegeztetés relatív indikációi ARF-ben a COPD súlyosbodása hátterében:
1) légzésszám >35/perc;
2) az artériás vér pH-ja<7,25;
3) PaO2<45 мм рт. ст., несмотря на проведение кислородотерапии.
Általános szabály, hogy a légzéstámogatás felírásakor átfogó klinikai és funkcionális értékelést végeznek a beteg állapotáról. A gépi lélegeztetésről való leszoktatást a lehető legkorábban el kell kezdeni a COPD-ben szenvedő betegeknél (B, 2++), mert minden további invazív légzéstámogatás jelentősen növeli a gépi lélegeztetés szövődményeinek kockázatát, különösen, mint a lélegeztetőgépes tüdőgyulladás (A, 1+) .
Mobilizálási és eltávolítási módszerek
hörgő szekréció
A szekréció túltermelése és a rossz légúti evakuálás komoly problémát jelenthet a COPD súlyos exacerbációjában szenvedő betegek számára.
A legújabb vizsgálatok szerint a mukoaktív gyógyszerekkel (acetilcisztein, karbocisztein, erdostein) végzett terápia felgyorsítja a COPD exacerbációinak rendeződését, és további hozzájárulást jelent a szisztémás gyulladások súlyosságának csökkentéséhez (C, 2+).
A COPD exacerbációjával a légutak elvezető funkcióját fokozó speciális módszerekkel jelentős állapotjavulás érhető el. Például a nagyfrekvenciás ütős lélegeztetés egy légzésterápiás módszer, amelynek során kis mennyiségű levegőt („ütőhangok”) juttatnak a páciensbe nagy beállítható frekvencián.
(60-400 ciklus / perc) és szabályozott nyomásszint egy speciális nyitott légzőkörön (fazitron) keresztül. Az "ütőhangszerek" maszkon, szájcsövön, endotracheális tubuson és tracheostomián keresztül adhatók. Egy másik módszer a mellkasfal nagyfrekvenciás oszcillációja (oszcillációja), amely a mellkason keresztül a légutakba és a rajtuk áthaladó gázáramba jut. A magas frekvenciájú rezgéseket egy felfújható mellény hozza létre, amely szorosan illeszkedik a mellkas köré és egy légkompresszorhoz van csatlakoztatva.
11. COPD és társbetegségek
A COPD, a magas vérnyomás, a koszorúér-betegség és a cukorbetegség mellett a krónikus betegségek vezető csoportját alkotják – az összes többi emberi patológia több mint 30%-át teszik ki. A COPD-t gyakran ezekkel a betegségekkel kombinálják, ami jelentősen ronthatja a betegek prognózisát.
A COPD leggyakoribb társbetegségeit a 20. táblázat mutatja be.
COPD-s betegeknél a halálozás kockázata az egyidejű betegségek számának növekedésével nő, és nem függ a FEV1 értéktől (3. ábra).
A COPD-s betegek összes halálozási okát a 21. táblázat tartalmazza.
Nagy populációs vizsgálatok szerint a COPD-ben szenvedő betegek szív- és érrendszeri betegségből eredő halálozási kockázata 2-3-szorosára nő az azonos korcsoportba tartozó, COPD-s betegekhez képest, és az összes halálozás körülbelül 50%-a.
A szív- és érrendszeri patológia a COPD-t kísérő fő patológia. Valószínűleg ez a COPD-vel párhuzamosan előforduló leggyakoribb és legsúlyosabb betegségek csoportja. Közülük meg kell különböztetni a koszorúér-betegséget, a krónikus szívelégtelenséget, a pitvarfibrillációt, a magas vérnyomást, amely nyilvánvalóan a COPD leggyakoribb kísérője.
Az ilyen betegek kezelése gyakran ellentmondásossá válik: a koszorúér-betegség és/vagy magas vérnyomás kezelésére alkalmazott gyógyszerek (angiotenzin-konvertáló enzim-gátlók, β-blokkolók) ronthatják a COPD lefolyását (köhögés, légszomj kialakulásának kockázata, megjelenése ill. a hörgőelzáródás fokozódása), valamint a COPD-re felírt gyógyszerek (hörgőtágítók, kortikoszteroidok), hátrányosan befolyásolhatják a szív- és érrendszeri betegségek lefolyását (szívritmuszavar kialakulásának kockázata, vérnyomás-emelkedés). Mindazonáltal a COPD-ben szenvedő betegek szív- és érrendszeri betegségének kezelését az általános ajánlásoknak megfelelően kell végezni, mivel nincs bizonyíték arra, hogy COPD jelenlétében eltérően kellene kezelni őket. Ha egyidejű kardiovaszkuláris patológiás COPD-s betegeknek β-blokkolókat kell felírni, előnyben kell részesíteni a szelektív β-blokkolókat.
A csontritkulás és a depresszió fontos társbetegségek, amelyeket gyakran aluldiagnosztizálnak. Ezek azonban az egészségi állapot romlásával és rossz prognózissal járnak. Kerülni kell a szisztémás kortikoszteroidok ismételt kezelését súlyosbodás esetén, mivel ezek alkalmazása jelentősen növeli a csontritkulás és a törések kockázatát.
Az utóbbi években egyre gyakoribbá váltak a metabolikus szindróma és a cukorbetegség kombinációjának esetei COPD-s betegeknél. A DM jelentős hatással van a COPD lefolyására, és rontja a betegség prognózisát. A 2-es típusú cukorbetegséggel kombinált COPD-ben szenvedő betegeknél a DN kifejezettebb, az exacerbációk gyakoribbak, a szívkoszorúér-betegség súlyosabb lefolyása, krónikus szívelégtelenség és magas vérnyomás figyelhető meg, a pulmonális hipertónia a hiperinfláció kisebb súlyosságával nő.
Az enyhe COPD-s betegeknél a leggyakoribb halálok a tüdőrák. Súlyos COPD-ben szenvedő betegeknél a csökkent tüdőfunkció jelentősen korlátozza a tüdőrák műtéti lehetőségét.
12. Rehabilitáció és betegoktatás
A COPD-s betegek kezelésének egyik javasolt kiegészítő módszere a betegség II. stádiumától kezdve a tüdőrehabilitáció. Hatékonynak bizonyult a testedzéstűrés (A, 1++), a napi aktivitás javításában, a nehézlégzés (A, 1++), a szorongás és a depresszió (A, 1+) észlelésének csökkentésében, valamint a a kórházi kezelések időtartama (A, 1 ++), a kórházból való kibocsátás utáni felépülési idő és általában a QoL (A, 1++) és a túlélés (B, 2++) növekedése.
A tüdőrehabilitáció egy átfogó, betegközpontú terápián alapuló beavatkozási program, amely a fizikai felkészítésen túl olyan oktatási és pszichoszociális programokat is tartalmaz, amelyek célja a betegek fizikai és érzelmi állapotának javítása, valamint a beteg magatartásának hosszú távú betartása. az egészség megőrzésében.
A 2013-as ERS/ATS ajánlások szerint a rehabilitációs tanfolyamot 1-ig kell folytatni
6-12 hét (legalább 12 óra, 2 rubel / hét, 30 percig vagy tovább), és a következő összetevőket tartalmazza:
1) fizikai edzés;
2) a tápláltsági állapot korrekciója;
3) betegoktatás;
4) pszichoszociális támogatás.
Ez a program járóbeteg alapon és kórházi körülmények között is végrehajtható.
A tüdőrehabilitáció fő összetevője a fizikai edzés, amely növelheti a hosszú hatású hörgőtágítók (B, 2++) hatékonyságát. Különösen fontos a végrehajtásuk integrált megközelítése, amely az erő- és állóképességi gyakorlatokat ötvözi: séta, a felső és alsó végtag izomzatának edzése expanderek, súlyzók, léptetőgépek segítségével, gyakorlatok kerékpár-ergométeren. Ezeken az edzéseken az ízületek különböző csoportjait is bevonják a munkába, fejlődik a kéz finommotorikája.
Minden gyakorlatot kombinálni kell légzőgyakorlatokkal, amelyek célja a helyes légzési minta kialakítása, ami további előnyökkel jár (C, 2+). Ezenkívül a légzőtornának tartalmaznia kell speciális szimulátorok (Threshold PEP, IMT) használatát, amelyek eltérően vonják be a belégzési és a kilégzési légzőizmokat a munkába.
A tápláltsági állapot korrekciójának az izomerő fenntartására kell irányulnia elegendő fehérje és vitamin bevitelével az étrendben.
A fizikai rehabilitáció mellett nagy figyelmet kell fordítani a betegek magatartásának megváltoztatására irányuló tevékenységekre, megtanítva nekik a betegség lefolyásában bekövetkezett változások önfelismerésének készségeit és korrekciós módszereit.
* Krónikus légúti betegségek, Útmutató az alapellátó orvosoknak, 2005.















A kezelés fő célja a betegség progressziójának megakadályozása. A kezelési célok a következők (12. táblázat)
12. táblázat A kezelés fő céljai
A kezelés fő irányai:
I. Nem farmakológiai hatások
- A kockázati tényezők hatásának csökkentése.
- · Oktatási programok.
II. Orvosi kezelés
Az expozíció nem gyógyszeres módszereit a 13. táblázat mutatja be.
13. táblázat: Az expozíció nem gyógyszeres módszerei
Súlyos betegségben (GOLD 2-4) szenvedő betegeknél szükséges intézkedésként tüdőrehabilitációt kell alkalmazni.
II. Orvosi kezelés
A gyógyszeres terápia mennyiségének megválasztása a klinikai tünetek súlyosságától, a hörgőtágító utáni FEV1 értékétől és a betegség súlyosbodásának gyakoriságától függ.
14. táblázat: A gyógyszeres terápia elvei stabil COPD-s betegekben a bizonyítékok szintjei szerint
|
Drogosztály |
Kábítószer-használat (bizonyítékok szintjével) |
|
Hörgőtágítók |
A bronchodilatátorok a COPD kezelésének alappillérei. (A, 1+) Inhalációs terápia előnyös. A gyógyszereket vagy „igény szerint”, vagy szisztematikusan írják fel. (A,1++) Előnyben részesítik a hosszú hatású hörgőtágítókat. (A, 1+) tiotropium-bromid, 24 órás hatású, csökkenti az exacerbációk és kórházi kezelések gyakoriságát, javítja a tüneteket és az életminőséget (A, 1++), javítja a tüdőrehabilitáció hatékonyságát (B, 2++) Formoterol és szalmeterol jelentősen javítja a FEV1-et és más tüdőtérfogatokat (QoL), csökkenti a tünetek súlyosságát és az exacerbációk gyakoriságát anélkül, hogy befolyásolná a mortalitást és a tüdőfunkció csökkenést. (A, 1+) Ultra hosszú hatású hörgőtágító indakaterol lehetővé teszi a FEV1 jelentős növelését, a légszomj súlyosságának, az exacerbációk gyakoriságának csökkentését és a QOL növelését. (A, 1+) |
|
Hörgőtágítók kombinációi |
A hosszú hatású hörgőtágítók kombinációi növelik a kezelés hatékonyságát, csökkentik a mellékhatások kockázatát, és nagyobb hatást fejtenek ki a FEV1-re, mint bármelyik gyógyszer önmagában. (B, 2++) |
|
Inhalációs glükokortikoszteroidok (iGCS) |
Kedvezően hatnak a betegség tüneteire, a tüdő működésére, az életminőségre, csökkentik az exacerbációk gyakoriságát, anélkül, hogy befolyásolnák a FEV1 fokozatos csökkenését, és nem csökkentik az általános mortalitást. (A, 1+) |
|
Az iGCS kombinációi hosszú hatású hörgőtágítókkal |
Az ICS-sel és hosszan ható β2-agonistákkal kombinált terápia csökkentheti a COPD-s betegek mortalitását. (B, 2++) Az ICS-sel és hosszan ható β2-agonistákkal kombinált terápia növeli a tüdőgyulladás kialakulásának kockázatát, de nincs más mellékhatása. (A, 1+) Kiegészítés a hosszú hatású β2-agonista és az ICS kombinációjához tiotropium-bromid javítja a tüdőfunkciót, az életminőséget és megelőzheti az ismétlődő exacerbációkat. (B, 2++) |
|
4-es típusú foszfodiészteráz inhibitorok |
Roflumilast csökkenti a mérsékelt és súlyos exacerbációk gyakoriságát a COPD súlyos és rendkívül súlyos lefolyású bronchitis-változatában szenvedő betegeknél, akiknek az anamnézisében exacerbáció szerepel. (A, 1++) |
|
Metilxantinok |
COPD-vel teofillin mérsékelt hörgőtágító hatása van a placebóhoz képest. (A, 1+) Teofillin alacsony dózisban csökkenti a COPD-s betegek exacerbációinak számát, de nem növeli a hörgőtágulás utáni tüdőfunkciót. (B, 2++) |
15. táblázat Az Oroszországban bejegyzett és a COPD-s betegek alapterápiájában használt alapvető gyógyszerek listája
|
Előkészületek |
egyszeri adagok |
hatás időtartama, |
||
|
Belégzésre (eszköz, mcg) |
Porlasztó terápia esetén mg/ml |
belül, mg |
||
|
c2-agonisták |
||||
|
rövid hatású |
||||
|
Fenoterol |
100-200 (DAI1) |
|||
|
Salbutamol |
||||
|
Hosszú hatású |
||||
|
Formoterol |
4,5–12 (DAI, DPI2) |
|||
|
Indakaterol |
150-300 (DPI) |
|||
|
Antikolinerg gyógyszerek |
||||
|
rövid hatású |
||||
|
Ipratropium-bromid |
||||
|
Hosszú hatású |
||||
|
Tiotropium-bromid |
|
|||
|
Glikopirrónium-bromid |
||||
|
Rövid hatású β2-agonisták + antikolinerg szerek kombinációja |
||||
|
fenoterol/ Ipratropia |
100/40-200/80 (DAI) |
|||
|
szalbutamol/ Ipratropia |
||||
|
Metilxantinok |
||||
|
teofillin (SR)*** |
Különféle, 24-ig |
|||
|
Inhalációs glükokortikoszteroidok |
||||
|
beklometazon |
||||
|
Budezonid |
100, 200, 400 (DPI) |
|||
|
flutikazon-propionát |
||||
|
Hosszú hatású β2-agonisták + glükokortikoszteroidok kombinációja egy inhalátorban |
||||
|
formoterol/ Budezonid |
|
|||
|
szalmeterol/ Flutikazon |
|
|||
|
4-foszfodiészteráz inhibitorok |
||||
|
Roflumilast |
1DAI - mért dózisú aeroszolos inhalátor; 2DPI - mért dózisú por inhalátor
A COPD-ben szenvedő betegek gyógyszeres terápiájának sémája a COPD súlyosságának átfogó értékelésén alapul (a betegség súlyosbodásának gyakorisága, a klinikai tünetek súlyossága, a COPD stádiuma, amelyet a hörgők átjárhatóságának mértéke határoz meg). a 16. táblázatban.
16. táblázat: COPD farmakológiai kezelési rendek (GOLD 2013)
|
COPD-s betegek |
Választható gyógyszerek |
Alternatív drogok |
Egyéb gyógyszerek |
|
COPD, enyhe (hörgőtágulás utáni FEV1 ≥ 50% előrejelzett) alacsony exacerbáció és ritka tünetek kockázatával (A csoport) |
1. séma: KDAH "igény szerint" 2. séma: KDBA "igény szerint" |
1. séma: 2. séma: 3. séma: összefüggésben a KDAH |
1) Teofillin |
|
COPD, nem súlyos (hörgőtágulás utáni FEV1 ≥ 50% előrejelzett), alacsony exacerbáció és gyakori tünetek kockázatával (B csoport) |
1. séma: 2. séma: |
1. séma: összefüggésben a DDBA |
és/vagy 2) Teofillin |
|
< 50% от должной) с высоким риском обострений и редкими симптомами (C csoport) |
1. séma: DDBA/IGKS 2. séma: |
1. séma: összefüggésben a DDBA 2. séma: összefüggésben a PDE-4 inhibitor 3. séma: összefüggésben a PDE-4 inhibitor |
és/vagy 2) Teofillin |
|
COPD, súlyos (hörgőtágítás utáni FEV1< 50% от должной) с высоким риском обострений и частыми симптомами (D csoport) |
1. séma: DDBA/IGKS 2. séma: Az 1. rendszer gyógyszerei mellett: 3. séma: |
1. séma: DDBA/IGKS összefüggésben a DDAH 2. séma: DDBA/IGKS összefüggésben a PDE-4 inhibitor 3. séma: összefüggésben a DDBA 4. séma : összefüggésben a PDE-4 inhibitor |
és/vagy 3) Teofillin |
*- KDAH - rövid hatású antikolinerg szerek; SABA - rövid hatású β2-agonisták; DDBA - hosszan ható β2-agonisták; DDAH - hosszú hatású antikolinerg szerek; IGCS - inhalációs glükokortikoszteroidok; PDE-4 – foszfodiészteráz inhibitorok – 4.
Egyéb kezelések: oxigénterápia, lélegeztetés támogatása és műtéti kezelés.
Oxigénterápia
A hosszú távú (napi 15 óra feletti) oxigénbevitel növeli a túlélést krónikus légzési elégtelenségben és súlyos nyugalmi hipoxémiában szenvedő betegeknél (B, 2++).
szellőzés támogatás
A nem invazív lélegeztetést széles körben alkalmazzák rendkívül súlyos és stabil COPD-ben szenvedő betegeknél.
A NIV és a hosszú távú oxigénterápia kombinációja hatásos lehet kiválasztott betegeknél, különösen azoknál, akiknek nyilvánvaló nappali hypercapniája van.
Sebészet:
Tüdőtérfogat-csökkentő műtét (LVA) és tüdőtranszplantáció.
A műtétet a tüdő egy részének eltávolításával hajtják végre a hiperinfláció csökkentése és a légzőizmok hatékonyabb pumpálása érdekében. Alkalmazását felső lebeny emfizémában és alacsony terheléstűrő betegeknél végzik.
A tüdőtranszplantáció javíthatja a gondosan kiválasztott, nagyon súlyos COPD-s betegek életminőségét és funkcionális teljesítményét. A kiválasztási kritériumok a FEV1<25% от должной величины, РаО2 <55 мм рт.ст., РаСО2 >50 Hgmm szobalevegő belégzéskor és pulmonalis hypertonia (Pra > 40 Hgmm).
2017. január 27 Megjelent az új COPD Globális Diagnosztikai, Kezelési és Prevenciós Stratégia (GOLD) munkacsoport 2017. évi jelentése, amely a krónikus obstruktív tüdőbetegség (COPD) területén 22 szakértő együttműködésével készült. Ez a jelentés a témában 2016 októberéig megjelent tudományos publikációkon alapul. Ezzel egyidejűleg megjelent online az American Journal of Respiratory and Critical Care Medicine folyóiratban, és a GOLD webhelyén is helyet kapott. A frissített iránymutatások áttekintik a diagnózis, a deeszkalációs stratégiák, a nem gyógyszeres kezelési lehetőségek, valamint a társbetegségek szerepét a COPD-s betegek kezelésében a legújabb fejleményeket.
A korábbiakhoz hasonlóan az új jelentés COPD-szűrést javasol azoknál a betegeknél, akiknek anamnézisében COPD-kockázati tényezők szerepelnek, valamint olyan betegeknél, akiknél légszomj, krónikus köhögés vagy köpet képződik. Ebben az esetben diagnosztikai kritériumként a hörgőtágító belélegzése utáni kényszerített kilégzési térfogat (FEV1) és a kényszerített vitálkapacitás (FVC) arányát javasolt használni diagnosztikai kritériumként.< 0,70. Факторами риска развития ХОБЛ считаются отягощенный семейный анамнез, низкая масса тела при рождении, частые респираторные инфекции в детстве, а также воздействие табачного дыма, дыма от сгорания топлива, которое используется для обогрева или приготовления пищи, а также ряд профессиональных воздействий, например, пыли, паров, копоти и прочих химических факторов.
Az új dokumentum egyik legfontosabb változása a tünetértékelés és a spirometriás vizsgálat elválasztása. Bár a tüdőfunkciós vizsgálat továbbra is szükséges a diagnózishoz, a vizsgálat fő célja a tünetek, az exacerbációk kockázatának, valamint a betegségnek a betegek általános egészségi állapotára gyakorolt hatásának felmérése. Ezen paraméterek alapján a betegek ezután A, B, C és D csoportokba sorolhatók, amelyek szerint a kezelést előírják. Így a spirometria továbbra is diagnosztikai eszköz és az obstrukció súlyosságának markere, de a farmakoterápiás döntésekhez már nincs szükség rá, kivéve a roflumilaszt felírását. A spirometriával meghatározott küszöbértékek továbbra is relevánsak a nem gyógyszeres terápiák, különösen a tüdőtérfogat-csökkentés és a tüdőtranszplantáció esetében.
Egy másik változás a súlyosbodás fogalmát érinti, amely most egyszerűbben és gyakorlatiasabban fogalmazódik meg. Az exacerbáció-megelőzés kezelésének evidenciáját is kiegészítették.
A GOLD jelentés másik új aspektusa a kezelés intenzifikációs és de-eszkalációs stratégiáinak részletes tárgyalása, míg a korábbi jelentések főként a kezdeti terápiás ajánlásokra összpontosítottak. A kezelési amplifikációs és deintenzifikációs algoritmusok bevonásával a szakértők módosították a kezelési lehetőségek tárgyalását, és kivették az első sort az alternatív terápiás lehetőségek közül. A dokumentum további indoklást tartalmaz az ajánlott kezdeti terápiához és a lehetséges alternatívákhoz az összes betegkategóriához (ABCD). Az irányelvek nagy hangsúlyt fektetnek a kombinált hörgőtágítók alkalmazására is, mint első vonalbeli kezelésre.
A frissített útmutató részletes elemzést ad a nem gyógyszeres kezelési lehetőségekről az influenza és a pneumococcus elleni védőoltáson túl az alsó légúti fertőzések kockázatának csökkentése érdekében. A dohányzás abbahagyása továbbra is minden kezelési terv legfontosabb szempontja, és a tüdőrehabilitáció rendkívül előnyös beavatkozás. Utóbbi alatt a páciens állapotának alapos felmérésén alapuló, szükségleteihez igazodó komplex beavatkozást értünk. Tartalmazhat olyan összetevőket, mint a testedzés, az oktatás (beleértve az önsegítést), a viselkedésbeli változások elérését célzó beavatkozások a fizikai és pszichológiai jólét javítása, valamint a kezeléshez való ragaszkodás fokozása érdekében. A tüdőrehabilitáció csökkentheti a közelmúltban bekövetkezett súlyosbodást követően a betegek visszafogadási és halálozási kockázatát, de bizonyíték van arra, hogy a beteg elbocsátása előtti megkezdése a mortalitás növekedéséhez vezethet.
Az oxigén inhaláció javíthatja a túlélést súlyos nyugalmi hipoxémiában szenvedő betegeknél, de a hosszú távú oxigénterápia stabil COPD-ben és közepesen súlyos vagy csak testmozgást igénylő hipoxémiában szenvedő betegeknél nem hosszabbítja meg a várható élettartamot, és nem csökkenti a kórházi kezelés kockázatát. Az asszisztált lélegeztetés hasznossága továbbra sem tisztázott, bár a bizonyítottan obstruktív alvási apnoéban szenvedő betegeknek folyamatos pozitív légúti nyomású gépeket kell használniuk a túlélés növelése és a kórházi kezelés kockázatának csökkentése érdekében.
Mint fentebb említettük, az új dokumentum fontos részét a COPD-s betegek társbetegségeinek diagnosztizálásának és kezelésének szentelték. A GOLD Jelentés az obstruktív alvási apnoe azonosításának és kezelésének fentebb tárgyalt fontosságán túl a komorbid szív- és érrendszeri betegségek, a csontritkulás, a szorongás és depresszió, a gastrooesophagealis reflux és ezek megfelelő kezelésének fontosságáról beszél.
A korábbi beszámolókhoz képest részletesebben tárgyaljuk a hatékonynak bizonyult sebészeti technikákat, mint a tüdőtérfogat-csökkentő műtét, bullectomia, tüdőtranszplantáció és egyes bronchoszkópos beavatkozások. A megfelelő indikációkkal rendelkező kiválasztott betegeknél mindezt figyelembe kell venni.
A palliatív ellátásról szóló rész is részletesebb lett. Megvitatja a hospice ellátást és más életvégi problémákat, valamint az olyan tünetek kezelésének optimális stratégiáit, mint a légszomj, fájdalom, szorongás, depresszió, fáradtság és alultápláltság.
Az új GOLD jelentések elvileg évente, szükség szerint jelennek meg, de a szöveg csak néhány évente változik jelentős mértékben, mivel jelentős mennyiségű új információ halmozódik fel, amelyet figyelembe kell venni a klinikai gyakorlatban. Ez a frissítés egy újabb ütemezett nagyobb átdolgozás eredménye, és a szerzők remélik, hogy munkájuk eredményeként az irányelvek praktikusabbak és könnyebben használhatók lesznek a különböző klinikai helyzetekben.
A COPD kezelés céljai 4 fő csoportra oszthatók:
A tünetek enyhítése és az életminőség javítása;
A jövőbeli kockázatok csökkentése stb. exacerbációk megelőzése;
A betegség progressziójának lassítása;
Csökkent mortalitás.
A COPD terápia farmakológiai és nem gyógyszeres megközelítéseket tartalmaz. A gyógyszeres kezelések közé tartoznak a hörgőtágítók, az ICS és a hosszú hatású hörgőtágítók (LABD) kombinációi, a foszfodiészteráz-4 inhibitorok, a teofillin, valamint az influenza és pneumococcus elleni védőoltások.
A nem gyógyszeres lehetőségek közé tartozik a dohányzás abbahagyása, a tüdő rehabilitációja, az oxigénterápia, a légzéstámogatás és a műtéti kezelés.
A COPD exacerbációinak kezelését külön mérlegeljük.
3.1 Konzervatív kezelés.
Leszokni a dohányzásról.
A dohányzás abbahagyása minden COPD-s beteg számára javasolt.Hozzászólások. A dohányzás abbahagyása a leghatékonyabb beavatkozás, amely a legnagyobb hatással van a COPD progressziójára. Az orvos szokásos tanácsa a betegek 7,4%-ánál vezet a dohányzás abbahagyásához (2,5%-kal több, mint a kontrolloknál), és egy 3-10 perces konzultáció eredményeként a dohányzás abbahagyásának gyakorisága eléri a 12%-ot. Több idővel és összetettebb beavatkozásokkal, ideértve a képességfejlesztést, a problémamegoldó tréninget és a pszichoszociális támogatást, a dohányzás abbahagyási aránya elérheti a 20-30%-ot.
Ellenjavallatok hiányában a dohányzás abbahagyására irányuló törekvések támogatására a dohányfüggőség kezelésére szolgáló gyógyszeres szerek javasoltak.
Hozzászólások. A farmakoterápia hatékonyan támogatja a dohányzás abbahagyására irányuló törekvéseket. A dohányfüggőség kezelésére szolgáló első vonalbeli gyógyszerek közé tartozik a vareniklin, a nyújtott hatóanyag-leadású bupropion és a nikotinpótló gyógyszerek.
Az orvosi tanácsok, támogató csoportok, készségfejlesztés és nikotinpótló terápia kombinációja a dohányzás abbahagyását 35%-ban eredményezi 1 év után, míg 22%-uk nemdohányzó marad 5 év után.
A stabil COPD gyógyszeres kezelésének alapelvei.
A COPD kezelésében használt gyógyszerek farmakológiai osztályait a táblázat tartalmazza. 5.
5. táblázat A COPD kezelésében használt gyógyszerek farmakológiai osztályai.
| Farmakológiai osztály | Előkészületek |
| KDBA | Salbutamol Fenoterol |
| DDBA | Vilanterol Indakaterol Szalmeterol Olodaterol Formoterol |
| KDAH | Ipratropium-bromid |
| DDAH | Aklidinium-bromid Glikopirrónium-bromid Tiotropium-bromid Umeklidinium-bromid |
| IGCS | Beklometazon Budezonid Mometazon Flutikazon Flutikazon Furoát Ciklezonid |
| Rögzített DDAH/DDBA kombinációk | Glikopirrónium-bromid/indakaterol Tiotropium-bromid/olodaterol Umeklidinium-bromid/vilanterol Aklidinium-bromid/formoterol |
| Az ICS/LABA rögzített kombinációi | Beklometazon/formoterol Budezonid/formoterol Flutikazon/szalmeterol Flutikazon-furoát/vilanterol |
| Foszfodiészteráz-4 inhibitorok | Roflumilast |
| Egyéb | Teofillin |
Jegyzet. SABA - rövid hatású β2-agonisták, KDAH - rövid hatású antikolinerg szerek, LABA - hosszú hatású β2-agonisták, DDAC - hosszú hatású antikolinerg szerek.
A farmakoterápia felírásakor javasolt a tünetkontroll elérését és a jövőbeni kockázatok csökkentését célozni - td; COPD exacerbációk és mortalitás (D5. függelék) .
Hozzászólások. A kezelés folytatása vagy befejezése a jövőbeni kockázatok (exacerbációk) csökkentése alapján javasolt. Ennek az az oka, hogy nem ismert, hogy egy gyógyszernek a tüdőfunkciót javító vagy a tüneteket csökkentő képessége hogyan korrelál a COPD exacerbációinak kockázatát csökkentő képességével. A mai napig nincs erős bizonyíték arra vonatkozóan, hogy bármely konkrét gyógyszeres terápia lelassítaná a betegség progresszióját (a minimális FEV1 csökkenés átlagos sebességével mérve) vagy csökkentené a mortalitást, bár az előzetes adatok ilyen hatásokra utalnak.
Hörgőtágítók.
A hörgőtágítók közé tartoznak a β2-agonisták és antikolinerg szerek, beleértve a rövid hatású (hatás időtartama 3-6 óra) és a hosszú hatású (hatás időtartama 12-24 óra) gyógyszereket.
Minden COPD-s betegnek rövid hatású hörgőtágítót kell adni, szükség szerint.
Az A ajánlások meggyőzési szintje (a bizonyítékok szintje - 1).
Hozzászólások. Rövid hatású hörgőtágítók alkalmazása is lehetséges az LABD-vel kezelt betegeknél. Ugyanakkor a DDBD-t kapó betegeknél a rövid hatású hörgőtágítók nagy dózisú rendszeres alkalmazása (beleértve a porlasztót is) nem indokolt, és csak a legnehezebb esetekben szabad alkalmazni. Ilyen helyzetekben átfogóan fel kell mérni a DDBD használatának szükségességét és a beteg azon képességét, hogy helyesen végezzen belégzést.
β2-agonisták.
A COPD kezelésére a következő hosszan ható β2-agonisták (LABA) alkalmazása javasolt: formoterol, szalmeterol, indakaterol, olodaterol (D6. melléklet).
Az ajánlás erősségi szintje A (bizonyítási szint - 1).
Hozzászólások. A FEV1-et és a nehézlégzést befolyásoló indakaterol és olodaterol legalább olyan jó, mint a formoterol, a szalmeterol és a tiotropium-bromid. A közepesen súlyos/súlyos exacerbációk kockázatára gyakorolt hatásukat tekintve a LABA (indakaterol, szalmeterol) gyengébb, mint a tiotropium-bromid.
A COPD-ben szenvedő, egyidejű szív- és érrendszeri megbetegedésekben szenvedő betegek kezelésében a LABA felírása előtt javasolt felmérni a kardiovaszkuláris szövődmények kialakulásának kockázatát.
Hozzászólások. A szív β-adrenerg receptorainak aktiválása β2-agonisták hatására feltehetően ischaemiát, szívelégtelenséget, aritmiát okozhat, és növeli a hirtelen halál kockázatát is. A COPD-ben szenvedő betegeken végzett kontrollos klinikai vizsgálatok során azonban nem gyűjtöttek adatokat az aritmiák, a kardiovaszkuláris vagy az általános mortalitás gyakoriságának növekedéséről a β2-agonisták alkalmazásakor.
A COPD kezelésében az asztmától eltérően a LABA monoterápiaként (ICS nélkül) alkalmazható.
Antikolinerg gyógyszerek.
A COPD kezelésére a következő tartós hatású antikolinerg szerek (LDAC) javasoltak: tiotropium-bromid, aklidinium-bromid, glikopirrónium-bromid, umeklidinium-bromid (D6. melléklet).
Az A ajánlások meggyőzési szintje (a bizonyítékok szintje - 1).
Hozzászólások. A tiotropium-bromid rendelkezik a legnagyobb bizonyítékkal a DDAC között. A tiotropium-bromid javítja a tüdőfunkciót, enyhíti a tüneteket, javítja az életminőséget és csökkenti a COPD exacerbációinak kockázatát.
Az aklidinium-bromid és a glikopirrónium-bromid javítja a tüdőfunkciót, az életminőséget és csökkenti a mentőgyógyszerek szükségességét. A legfeljebb 1 évig tartó vizsgálatok során az aklidinium-bromid, a glikopirrónium-bromid és az umeklidinium-bromid csökkentette a COPD súlyosbodásának kockázatát, de a tiotropium-bromiddal végzett vizsgálatokhoz hasonló, hosszú távú, 1 évnél tovább tartó vizsgálatokat a mai napig nem végeztek.
Az inhalációs antikolinerg szerek általában jól tolerálhatók, és a mellékhatások (AE) viszonylag ritkák a használatuk során.
COPD-ben és egyidejű szív- és érrendszeri betegségben szenvedő betegeknél a DDAC alkalmazása javasolt.
Az A ajánlások meggyőzési szintje (a bizonyítékok szintje - 1).
Hozzászólások. Felmerült a gyanú, hogy a rövid hatású antikolinerg szerek (SAC) szívvel kapcsolatos nemkívánatos eseményeket okoznak, de nem érkezett jelentés a kardiális nemkívánatos események megnövekedett előfordulásáról a DDAC-okkal kapcsolatban. A 4 éves UPLIFT-vizsgálatban a tiotropium-bromiddal kezelt betegeknél szignifikánsan kevesebb kardiovaszkuláris esemény fordult elő, és az általános mortalitás is kisebb volt, mint a placebo-csoportban. A TIOSPIR-vizsgálatban (a kezelés átlagos időtartama 2,3 év) a tiotropium-bromid folyékony inhalátorban rendkívül biztonságosnak bizonyult, és nem különbözött a szárazpor-inhalátorban alkalmazott tiotropium-bromidtól a mortalitás, a súlyos szívbetegségek és a COPD exacerbációja tekintetében.
Hörgőtágító kombinációk.
Különböző hatásmechanizmusú hörgőtágítók kombinációja javasolt a nagyobb hörgőtágulás és a tünetek enyhítése érdekében.
Az A ajánlások meggyőzési szintje (a bizonyítékok szintje - 1).
Hozzászólások. Például a CAAC és a CABA vagy LABA kombinációja nagyobb mértékben javítja a FEV1-et, mint bármelyik monokomponens. A SABA vagy LABA adható DDAC-val kombinálva, ha a DDAA önmagában nem enyhíti a tüneteket.
A COPD kezelésére a DDAH / LABA rögzített kombinációinak alkalmazása javasolt: glikopirrónium-bromid / indakaterol, tiotropium-bromid / olodaterol, umeklidinium-bromid / vilanterol, aklidinium-bromid / formoterol.
Az A ajánlások meggyőzési szintje (a bizonyítékok szintje - 1).
Hozzászólások. Ezek a kombinációk előnyt mutattak a placebóval és monokomponenseikkel szemben a minimális FEV1-re, a nehézlégzésre és az életminőségre gyakorolt hatás tekintetében, és nem maradtak el náluk a biztonság tekintetében. A tiotropium-bromiddal összehasonlítva minden DDAC/LABA kombináció jobb hatást mutatott a tüdőfunkcióra és az életminőségre. A nehézlégzésre gyakorolt hatást tekintve az umeklidinium-bromid/vilanterol kombináció nem mutatott előnyt, és csak a tiotropium-bromid/olodaterol volt szignifikánsan jobb a tiotropium-bromid monoterápiánál a PHI-re gyakorolt hatás tekintetében.
Ugyanakkor a DDAC/LABA kombinációk még nem mutattak előnyt a tiotropium-bromid monoterápiával szemben a COPD mérsékelt/súlyos exacerbációinak kockázatára gyakorolt hatásuk tekintetében.
Inhalációs glükokortikoszteroidok és kombinációik β2-agonistákkal.
Az inhalációs kortikoszteroidok csak a folyamatban lévő DDBD-terápia mellett javasoltak olyan COPD-ben szenvedő betegeknél, akiknek anamnézisében BA szerepel, és véreozinofíliában szenved (a vérben az eozinofilek tartalma súlyosbodás nélkül több mint 300 sejt/1 μl).
A B ajánlások meggyőzési szintje (a bizonyítékok szintje - 1).
Hozzászólások. AD-ban az ICS terápiás és nemkívánatos hatásai az alkalmazott dózistól függenek, COPD-ben azonban nincs ilyen dózisfüggés, és a hosszú távú vizsgálatok során csak közepes és nagy dózisú ICS-t alkalmaztak. A COPD-s betegek ICS-kezelésre adott válaszát nem lehet előre megjósolni az orális kortikoszteroidokra adott válasz, a hörgőtágító teszt eredményei vagy a bronchiális túlérzékenység megléte alapján.
A COPD-ben és gyakori exacerbációban (2 vagy több közepesen súlyos exacerbáció 1 éven belül vagy legalább 1 súlyos exacerbáció, amely kórházi kezelést igényel) szenvedő betegeknek az LABD mellett ICS-t is fel kell írni.
A B ajánlások meggyőzési szintje (a bizonyítékok szintje - 1).
Hozzászólások. A hosszú távú (6 hónapos) ICS-kezelés és az ICS/LABA kombinációja csökkenti a COPD exacerbációinak gyakoriságát és javítja a betegek életminőségét.
Az ICS kettős (LABA/IGCS) vagy tripla (LAAA/LABA/IGCS) terápiaként használható. A hármas terápiát olyan vizsgálatokban tanulmányozták, ahol az ICS/LABA kombináció hozzáadása a tiotropium-bromid kezeléshez a tüdőfunkció javulását, az életminőség javulását, valamint az exacerbációk, különösen a súlyosak további csökkenését eredményezte. A hármas terápia azonban további tanulmányokat igényel hosszabb vizsgálatok során.
Az exacerbációk magas kockázatával és véreozinofíliával nem rendelkező COPD-ben szenvedő betegeknél, azonos fokú bizonyítékokkal, LAAC vagy IGCS / LABA felírása javasolt.
Az A ajánlások meggyőzési szintje (a bizonyítékok szintje - 1).
Hozzászólások. A COPD-ben szenvedő betegeknél az ICS kinevezésének fő várható hatása az exacerbációk kockázatának csökkenése. Ebből a szempontból az ICS/LABA nem jobb, mint a DDAH (tiotropium-bromid) monoterápia. A legújabb tanulmányok azt mutatják, hogy az ICS/LABA kombinációk előnye a hörgőtágítókkal szemben az exacerbációk kockázatára gyakorolt hatás szempontjából csak a véreozinofíliában szenvedő betegeknél van.
Azok a COPD-ben szenvedő betegek, akiknek a tüdőfunkciója megőrzött, és nem szerepel az anamnézisben visszatérő exacerbáció, nem javasolt az ICS alkalmazása.
A B ajánlások meggyőzési szintje (a bizonyítékok szintje - 1).
Hozzászólások. Az ICS-terápia és az ICS/LABA kombinációja nem befolyásolja a FEV1 és a mortalitás csökkenésének ütemét COPD-ben.
Tekintettel a súlyos mellékhatások kockázatára, az ICS alkalmazása COPD-ben nem javasolt a kezdeti terápia részeként.
A B ajánlások meggyőzési szintje (a bizonyítékok szintje - 1).
Hozzászólások. Az ICS nemkívánatos hatásai közé tartozik a szájüregi candidiasis és a rekedtség. Bizonyíték van a tüdőgyulladás, a csontritkulás és a törések fokozott kockázatára ICS és ICS/LABA kombinációk esetén. A tüdőgyulladás kockázata COPD-ben szenvedő betegeknél nem csak a flutikazon, hanem más ICS alkalmazása esetén is nő. Az ICS kezelés megkezdése a diabetes mellitus kialakulásának fokozott kockázatával járt légúti patológiás betegeknél.
Roflumilast.
A roflumilaszt a foszfodiészteráz-4 enzim gátlásával és a ciklikus adenozin-monofoszfát intracelluláris tartalmának növelésével elnyomja a COPD-vel kapcsolatos gyulladásos választ.
A roflumilaszt FEV1-es COPD-s betegek számára javasolt< 50% от должного, с хроническим бронхитом и частыми обострениями, несмотря на применение ДДБД для уменьшения частоты среднетяжелых и тяжелых обострений .
Az A ajánlások meggyőzési szintje (a bizonyítékok szintje - 1).
A roflumilast nem javasolt a COPD tüneteinek kezelésére.
Az A ajánlások meggyőzési szintje (a bizonyítékok szintje - 1).
Hozzászólások. A roflumilaszt nem hörgőtágító, bár a szalmeterolt vagy tiotropium-bromidot kapó betegek hosszú távú kezelése során a roflumilaszt emellett 50-80 ml-rel növeli a FEV1-et.
A roflumilaszt az életminőségre és a tünetekre gyakorolt hatása gyenge. A gyógyszer jelentős mellékhatásokat okoz, amelyek között jellemző a gyomor-bélrendszeri betegségek és a fejfájás, valamint a fogyás.
Orális glükokortikoszteroidok.
COPD-s betegeknél ajánlott kerülni a hosszú távú orális kortikoszteroid kezelést, mivel az ilyen kezelés ronthatja hosszú távú prognózisukat.
Hozzászólások. Bár az orális kortikoszteroidok nagy dózisa (amely napi ≥30 mg orális prednizolonnak felel meg) rövid távon javítja a tüdőfunkciót, az orális kortikoszteroidok alacsony, közepes és nagy dózisú hosszú távú alkalmazásának előnyeiről nem állnak rendelkezésre adatok. az AE kockázatának jelentős növekedése. Ez a tény azonban nem akadályozza meg az orális kortikoszteroidok kinevezését az exacerbációk során.
Az orális kortikoszteroidok számos súlyos nemkívánatos hatást okoznak; A COPD-vel kapcsolatban az egyik legfontosabb a szteroid myopathia, melynek tünetei az izomgyengeség, a csökkent fizikai aktivitás és a légzési elégtelenség rendkívül súlyos COPD-s betegeknél.
Teofillin.
Továbbra is vita folyik a teofillin pontos hatásmechanizmusáról, de ennek a gyógyszernek mind hörgőtágító, mind gyulladásgátló hatása van. A teofillin jelentősen javítja a tüdőfunkciót COPD-ben, és esetleg javítja a légzőizmok működését, de növeli a nemkívánatos események kockázatát. Bizonyíték van arra, hogy a teofillin alacsony dózisai (100 mg 2 r / nap) statisztikailag szignifikánsan csökkentik a COPD exacerbációinak gyakoriságát.
A teofillin a COPD kezelésére javasolt kiegészítő terápiaként súlyos tünetekkel küzdő betegeknél.
Hozzászólások. A teofillin hatása a tüdőfunkcióra és a COPD tüneteire kevésbé kifejezett, mint a LABA formoterolé és a szalmeterolé.
A teofillin pontos hatásának időtartama COPD-ben, beleértve a jelenlegi lassan felszabaduló készítményeket is, nem ismert.
A teofillin felírásakor ajánlott ellenőrizni annak koncentrációját a vérben, és a kapott eredményektől függően módosítani kell a gyógyszer adagját.
Az ajánlások meggyőző képességének szintje C (bizonyítási szint - 3).
Hozzászólások. A teofillin farmakokinetikáját az egyének közötti különbségek és a gyógyszerkölcsönhatásokra való hajlam jellemzik. A teofillin terápiás koncentráció-tartománya szűk, és toxicitáshoz vezethet. A leggyakoribb mellékhatások közé tartozik a gyomorirritáció, hányinger, hányás, hasmenés, fokozott diurézis, központi idegrendszeri stimuláció jelei (fejfájás, idegesség, szorongás, izgatottság) és szívritmuszavarok.
Antibakteriális gyógyszerek.
A makrolidok (azitromicin) kijelölése a hosszú távú terápia során ajánlott bronchiectasisban és gyakori gennyes exacerbációval járó COPD-ben szenvedő betegek számára.
Ajánlás erősségi szintje C (bizonyítási szint - 2).
Hozzászólások. Egy közelmúltban végzett metaanalízis kimutatta, hogy a makrolidokkal (eritromicin, klaritromicin és azitromicin) végzett hosszú távú kezelés 6, 3-12 hónapig tartó vizsgálatban 37%-kal csökkentette a COPD exacerbációinak gyakoriságát a placebóhoz képest. Emellett a kórházi kezelések száma 21%-kal csökkent. A makrolidok széles körű alkalmazását korlátozza a velük szembeni bakteriális rezisztencia növekedésének kockázata és a mellékhatások (halláskárosodás, kardiotoxicitás).
Mukoaktív gyógyszerek.
Ebbe a csoportba több különböző hatásmechanizmusú anyag tartozik. A mucolitikumok rendszeres használatát COPD-ben számos tanulmány vizsgálta ellentmondó eredményekkel.
Az N-acetil-cisztein és a karbocisztein kijelölése javasolt bronchitis fenotípusú és gyakori exacerbációjú COPD-s betegek számára, különösen akkor, ha az ICS-t nem kezelik.
Ajánlás erősségi szintje C (bizonyíték szintje - 3).
Hozzászólások. Az N-aceticisztein és a karbocisztein antioxidáns tulajdonságokat mutathatnak, és csökkenthetik az exacerbációkat, de nem javítják a tüdőfunkciót vagy az életminőséget COPD-s betegekben.
Az inhalátor kiválasztása.
Javasoljuk, hogy a COPD-ben szenvedő betegeket tájékoztassák az inhalátorok helyes használatáról a kezelés kezdetén, majd a későbbi vizitek alkalmával ellenőrizni kell a használatukat.Hozzászólások. A betegek jelentős része hibázik az inhalátorok használata során. Kimért dózisú porinhalátor (DPI) használatakor nincs szükség koordinációra a gomb megnyomása és a belégzés között, de elegendő belégzési erőfeszítés szükséges a megfelelő belégzési áramlás megteremtéséhez. Kimért dózisú aeroszolos inhalátor (MAI) használatakor nincs szükség nagy belégzési áramlásra, de a páciensnek képesnek kell lennie az inhalátor aktiválásának összehangolására a belégzés megkezdésével.
A PDI-k felírásakor távtartók használata javasolt, hogy kiküszöböljük a koordinációs problémát és csökkentsük a gyógyszer lerakódását a felső légutakban.
Az A ajánlások meggyőzési szintje (a bizonyítékok szintje - 3).
Súlyos COPD-ben szenvedő betegeknél ajánlatos előnyben részesíteni a PDI-t (beleértve a távtartót is) vagy a folyékony inhalátort.
Az A ajánlások meggyőzési szintje (a bizonyítékok szintje - 3).
Hozzászólások. Ez az ajánlás azon a tényen alapul, hogy a belégzési áramlás nem mindig elegendő súlyos COPD-ben szenvedő betegeknél DPI-t alkalmazva.
A megfelelő inhalátor kiválasztásának alapelveit a G7. függelék ismerteti.
Stabil COPD kezelése.
Minden COPD-s betegnek javasoljuk, hogy tegyen nem gyógyszeres intézkedéseket, írjon fel rövid hatású hörgőtágítót szükség szerint, oltson be influenza és pneumococcus fertőzés ellen, és kezelje a társbetegségeket.Hozzászólások. A nem gyógyszeres beavatkozások közé tartozik a dohányzás abbahagyása, az inhalációs technika és az önmenedzselés oktatása, az influenza és pneumococcus elleni védőoltások, a fizikai aktivitásra való ösztönzés, a hosszú távú oxigénterápia (VCT) és a non-invazív lélegeztetés (NIV) szükségességének felmérése.
Minden COPD-s betegnek javasoljuk, hogy monoterápiában írjon fel DDBD-t – DDAC/LABA kombinációt vagy ezen gyógyszerek valamelyikét (B függelék).
Az A ajánlások meggyőzési szintje (a bizonyítékok szintje - 1).
Ha a betegnek súlyos tünetei vannak (mMRC ≥ 2 vagy CAT ≥ 10), a COPD diagnózisának megállapítása után azonnal a LAAD/LABA kombináció felírása javasolt.
Az A ajánlások meggyőzési szintje (a bizonyítékok szintje - 1).
Hozzászólások. A legtöbb COPD-s beteg súlyos tünetekkel, például légszomjjal és csökkent edzéstűrőséggel jelentkezik. A DDAH / LABA kombináció kijelölése a maximális hörgőtágulás miatt lehetővé teszi a légszomj enyhítését, a terhelési tolerancia növelését és a betegek életminőségének javítását.
Tünetmentes betegeknél (mMRC) javasolt a monoterápia megkezdése egyetlen hosszú hatású hörgőtágítóval (LABA vagy LABA).< 2 или САТ.
Az A ajánlások meggyőzési szintje (a bizonyítékok szintje - 1).
Hozzászólások. A DDAH előnye, hogy kifejezettebb hatással van az exacerbációk kockázatára.
A tünetek (légszomj és csökkent terhelési tolerancia) tartós fennállása esetén, a kizárólag LABD-vel végzett monoterápia hátterében, javasolt a hörgőtágító terápia fokozása - át kell vinni a DDAH / LABA kombinációjára (B függelék).
A DDAH/LABA kombináció kijelölése monoterápia helyett ismételt exacerbációk (1 éven belül 2 vagy több mérsékelt exacerbáció vagy legalább 1 súlyos, kórházi kezelést igénylő exacerbáció) esetén is javasolt azoknál a betegeknél, akiknél nincs asztma indikációja és nem áll fenn véreozinofília (B függelék). .
Az A ajánlások meggyőzési szintje (a bizonyítékok szintje - 2).
Hozzászólások. A DDAC/LABA glikopirrónium-bromid/indakaterol kombinációja a FLAME vizsgálatban hatékonyabban csökkentette a COPD mérsékelt/súlyos exacerbációinak kockázatát, mint az ICS/LABA (flutikazon/szalmeterol) kombinációja azoknál a COPD-s betegeknél, akiknél a FEV1 25-60%-os előrejelzett és nem volt. magas vérszintű eozinofília.
Ha COPD-ben és BA-ban vagy véreozinofíliában szenvedő betegeknél ismétlődő exacerbációk lépnek fel a LABA önmagában történő terápia során, akkor a betegnek LABA / ICS felírása javasolt (B függelék).
Az A ajánlások meggyőzési szintje (a bizonyítékok szintje - 2).
Hozzászólások. A véreozinofília kritériuma az eozinofil tartalom a vérben (súlyosbodás nélkül) 300 sejt/1 µl.
Ha asztmában vagy eozinofíliában szenvedő COPD-ben szenvedő betegeknél ismétlődő exacerbációk lépnek fel a DDAC / LABA kombinációjával végzett terápia során, akkor a betegnek ICS hozzáadása javasolt (B függelék).
Az A ajánlások meggyőzési szintje (a bizonyítékok szintje - 2).
Hozzászólások. A beteg az IGCS/LABA terápia elégtelen hatékonyságával is hármas terápiára kerülhet, ha LAAA-t adnak a kezeléshez.
A LAAA/LABA/IGCS hármas terápiája jelenleg kétféleképpen adható: 1) LAAA/LABA rögzített kombinációja és külön ICS inhalátor alkalmazásával; 2) LABA/IGCS és különálló DDAH inhalátor rögzített kombinációjával. A módszerek közötti választás a kezdeti terápiától, a különböző inhalátoroknak való megfeleléstől és a gyógyszerek elérhetőségétől függ.
Ha asztmában és eozinofíliában nem szenvedő betegnél LAAA/LABA kombinációval végzett kezelés során ismételt exacerbáció vagy hármas terápia (LAHA/LABA/IGCS) exacerbációinak visszaesése esetén a COPD fenotípusának tisztázása és fenotípus-specifikus felírása javasolt. terápia (roflumilaszt, N-acetilcisztein, azitromicin stb. ; – B függelék).
A B ajánlások meggyőzési szintje (a bizonyítékok szintje - 3).
A hörgőtágító terápia volumenének csökkentése (AE hiányában) még a tünetek maximális enyhülése esetén sem javasolt.
Az A ajánlás ereje (bizonyítási szint -2).
Hozzászólások. Ez annak a ténynek köszönhető, hogy a COPD progresszív betegség, így a tüdőfunkció teljes normalizálása nem lehetséges.
Az ismétlődő exacerbációk nélküli COPD-ben szenvedő betegeknél, akiknek a tüdőfunkciója megmaradt (FEV1 az előrejelzett érték 50%-a), javasolt az ICS teljes leállítása, feltéve, hogy DDBD-t írnak fel.
Ajánlás erősségi szintje B (bizonyíték szintje -2).
Hozzászólások. Ha az orvos véleménye szerint a betegnek nem kell folytatnia az ICS-kezelést, vagy az ilyen kezelés során nemkívánatos események léptek fel, akkor az ICS az exacerbációk kockázatának növelése nélkül lemondható.
FEV1-es betegeknél< 50% от должного, получающих тройную терапию, рекомендуется постепенная отмена ИГКС со ступенчатым уменьшением его дозы в течение 3 месяцев .
Az A ajánlás erőssége (bizonyíték szintje -3).
Hozzászólások. FEV1 érték< 50% ранее считалось фактором риска частых обострений ХОБЛ и рассматривалось как показание к назначению комбинации ИГКС/ДДБА. В настоящее время такой подход не рекомендуется, поскольку он приводит к нежелательным эффектам и неоправданным затратам , хотя в реальной практике ИГКС и комбинации ИГКС/ДДБА назначаются неоправданно часто.
3.2 Sebészeti kezelés.
A tüdőtérfogat-csökkentő műtét a felső lebeny emfizémás és rossz terheléstűrő COPD-s betegek számára javasolt.Az ajánlások meggyőző képességének szintje C (bizonyítási szint - 3).
Hozzászólások. A tüdőtérfogat-csökkentő műtétet a tüdő egy részének eltávolításával hajtják végre a hiperinfláció csökkentése és a légzőizmok hatékonyabb pumpálása érdekében. Jelenleg a tüdő térfogatának csökkentésére kevésbé invazív módszerek is alkalmazhatók - a szegmentális hörgők elzárása szelepek, speciális ragasztó stb. segítségével;
Számos nagyon súlyos COPD-s beteg esetében javasolt a tüdőtranszplantáció a következő indikációk megléte esetén: BODE index ≥ 7 pont (BODE - B - testtömegindex (testtömegindex), O - obstrukció (elzáródás) D - nehézlégzés ( légszomj), E - edzéstűrés (fizikai aktivitás tolerancia)), FEV1< 15% от должных, ≥ 3 обострений в предшествующий год, 1 обострение с развитием острой гиперкапнической дыхательной недостаточности (ОДН), среднетяжелая-тяжелая легочная гипертензия (среднее давление в легочной артерии ≥35 мм) .
Az ajánlások meggyőző képességének szintje C (bizonyítási szint - 3).
Hozzászólások. A tüdőtranszplantáció javíthatja az életminőséget és a funkcionális teljesítményt gondosan kiválasztott COPD-s betegeknél.
3.3 Egyéb kezelések.
Hosszú távú oxigénterápia.
A COPD késői (terminális) stádiumában kialakuló egyik legsúlyosabb szövődménye a krónikus légzési elégtelenség (CRF). A krónikus veseelégtelenség fő tünete a hipoxémia stb. kialakulása; az artériás vér oxigéntartalmának csökkenése (PaO2).A VCT jelenleg azon kevés terápia egyike, amely csökkentheti a COPD-ben szenvedő betegek mortalitását. A hipoxémia nemcsak lerövidíti a COPD-s betegek életét, hanem további jelentős káros következményekkel is jár: az életminőség romlása, policitémia kialakulása, az alvás közbeni szívritmuszavarok fokozott kockázata, valamint a pulmonalis hypertonia kialakulása és progressziója. A VCT csökkentheti vagy megszüntetheti a hipoxémia mindezen negatív hatásait.
A VCT javasolt krónikus veseelégtelenségben szenvedő COPD-s betegek számára (javallatokat lásd a D8. mellékletben).
Az A ajánlás ereje (bizonyítási szint -1).
Hozzászólások. Hangsúlyozni kell, hogy a cor pulmonale klinikai tüneteinek jelenléte a VCT korábbi kinevezésére utal.
A hipoxémia oxigénnel történő korrekciója a CRD kezelésének patofiziológiailag leginkább alátámasztott módja. Számos sürgősségi esettel (tüdőgyulladás, tüdőödéma, trauma) ellentétben a krónikus hipoxémiában szenvedő betegek oxigénhasználatának állandónak, hosszan tartónak kell lennie, és általában otthon kell végezni, ezért ezt a terápiás formát VCT-nek nevezik.
A gázcsere paramétereit, amelyeken a VCT indikációi alapulnak, csak a betegek stabil állapota alatt javasolt értékelni stb.; 3-4 héttel a COPD súlyosbodása után.
Az ajánlások meggyőző képességének szintje C (bizonyítási szint - 3).
Hozzászólások. Ez az idő szükséges a gázcsere és az oxigénszállítás helyreállításához egy ODN időszak után. A COPD-s betegek VCT felírása előtt javasolt meggyőződni arról, hogy a gyógyszeres terápia lehetőségei kimerültek, és a lehetséges maximális terápia nem vezet a PaO2 határértékek fölé emelkedéséhez.
Az oxigénterápia felírásakor javasolt törekedni a 60 mm-es PaO2 és 90%-os SaO2 érték elérésére.
Az ajánlások meggyőző képességének szintje C (bizonyítási szint - 3).
A VCT nem javasolt olyan COPD-s betegek számára, akik továbbra is dohányoznak; nem részesül megfelelő gyógyszeres kezelésben a COPD lefolyásának szabályozására (hörgőtágítók, ICS); nem kellően motivált az ilyen típusú terápiára.
Az ajánlások meggyőző képességének szintje C (bizonyítási szint - 3).
A legtöbb COPD-s betegnek javasolt a VCT elvégzése legalább napi 15 órán keresztül, az ülések közötti maximális intervallumok nem haladhatják meg a 2 órát egymás után, 1-2 l/perc oxigénáramlás mellett.
A B ajánlások meggyőzési szintje (a bizonyítékok szintje - 2).
Hosszan tartó otthoni szellőztetés.
A hypercapnia (td; megnövekedett szén-dioxid részleges feszültség az artériás vérben - PaCO2 ≥ 45 mm) a lélegeztetési tartalék csökkenésének markere a tüdőbetegségek terminális stádiumában, és negatív prognosztikai tényezőként is szolgál a COPD-s betegek számára. Az éjszakai hypercapnia megváltoztatja a légzőközpont érzékenységét a CO2-ra, ami nappal magasabb PaCO2-szinthez vezet, ami negatív következményekkel jár a szív, az agy és a légzőizmok működésére nézve. A légzőizmok diszfunkciója a légzőkészülék nagy rezisztív, rugalmas és küszöbterhelésével kombinálva tovább súlyosbítja a COPD-s betegek hypercapniáját, így kialakul egy "ördögi kör", amelyet csak légzéstámogatás (pulmonális lélegeztetés) lehet megtörni.A krónikus veseelégtelenség stabil lefolyású COPD-s betegeknél, akik nem szorulnak intenzív ellátásra, lehetőség van a tartós otthoni légzéstámogatásra - az úgynevezett hosszú távú otthoni lélegeztetésre (LHVL).
A DDWL alkalmazása COPD-s betegeknél számos pozitív patofiziológiai hatással jár, amelyek közül a fő a gázcsere paraméterek javulása - a PaO2 növekedése és a PaCO2 csökkenése, a légzőizmok működésének javulása, a gyakorlati tolerancia növekedése, az alvásminőség javulása és az LHI csökkenése. A legújabb tanulmányok kimutatták, hogy a non-invazív tüdőlélegeztetés (NIV) megfelelően kiválasztott paramétereivel jelentős javulás lehetséges a hypercapnic CRD-vel szövődött COPD-s betegek túlélésében.
A DDWL olyan COPD-s betegek számára ajánlott, akik megfelelnek a következő kritériumoknak:
- A krónikus veseelégtelenség tüneteinek jelenléte: gyengeség, légszomj, reggeli fejfájás;
- Az alábbiak valamelyikének jelenléte: PaCO2 55 mm, PaCO2 50-54 mm és éjszakai deszaturációs epizódok (SaO2< 88% в течение более 5 мин во время O2-терапии 2 л/мин), PaCO2 50-54 мм и частые госпитализации вследствие развития повторных обострений (2 и более госпитализаций за 12 мес).
Az A ajánlások meggyőzési szintje (a bizonyítékok szintje - 1).
 Ha a férj ingerlékeny lett
Ha a férj ingerlékeny lett Tabletták a cukorbetegség számára
Tabletták a cukorbetegség számára Továbbá - kell-e vessző?
Továbbá - kell-e vessző? Hogyan készülnek a számítógépes játékok?
Hogyan készülnek a számítógépes játékok? Álomértelmezés arany, miért álmodik aranyról, álomban aranyról
Álomértelmezés arany, miért álmodik aranyról, álomban aranyról Húgyhólyaghurut húgycsőmosás Hogyan kell felhelyezni a szubklavia katétert
Húgyhólyaghurut húgycsőmosás Hogyan kell felhelyezni a szubklavia katétert Horoszkóp disznó és tigris. Tigris - Malac. Kompatibilitás
Horoszkóp disznó és tigris. Tigris - Malac. Kompatibilitás